Biologie [Ouvrage de référence complet pour la préparation à l'examen d'État unifié] Lerner Georgy Isaakovich
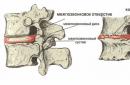
5.3.1. Environnement interne du corps. Composition et fonctions du sang. Groupes sanguins. Transfusion sanguine. Immunité
Termes et concepts de base testés dans les épreuves d'examen : anticorps, vaccin, environnement interne de l'organisme, immunité (naturelle, artificielle, active, passive, congénitale, acquise), lymphe, plasma, facteur Rh, fibrine, fibrinogène, cellules sanguines (leucocytes, lymphocytes, plaquettes, érythrocytes).
L'environnement interne du corps se forme sang, lymphe et liquide tissulaire.
Le métabolisme entre les cellules, la lymphe et le sang se fait par le biais du liquide tissulaire formé à partir du plasma sanguin. L'environnement interne du corps assure la communication humorale entre les organes. C'est relativement constant. La constance de l'environnement interne du corps est appelée homéostasie. Sang- la composante la plus importante de l'environnement interne. Il s'agit d'un tissu conjonctif liquide constitué d'éléments formés et de plasma.
Fonctions sanguines :
– transport– transporte et distribue des produits chimiques dans tout le corps ;
– protecteur– contient des anticorps, effectue la phagocytose des bactéries ;
– thermorégulateur– assure la répartition de la chaleur générée lors du métabolisme et son rejet dans le milieu extérieur ;
– respiratoire– assure les échanges gazeux entre les tissus, les cellules et le milieu interne.
Le corps adulte contient environ 5 litres de sang. Certains circulent dans les vaisseaux et d’autres se trouvent dans des dépôts sanguins.
Conditions pour un fonctionnement sanguin normal :
– le volume sanguin ne doit pas être inférieur à 7 % ;
– vitesse du flux sanguin – 5 l par minute;
– maintenir un tonus vasculaire normal.
Composition sanguine : plasma représente 55 % du volume sanguin, dont 90 à 92 % d'eau et 8 à 10 % de substances inorganiques et organiques.
La composition du plasma sanguin comprend : des protéines - albumine, globulines, fibrinogène, prothrombine. Le plasma dépourvu de fibrine est appelé sérum. pH plasmatique = 7,3-7,4.
Éléments formés du sang.
des globules rouges - des globules rouges. En 1 mm 3 4-5 millions.
Leucocytes – des globules blancs de 8 à 10 microns de diamètre. Dans 1 mm 3 5-8 mille.
Plaquettes – cellules anucléées (plaques de sang). Diamètre 5 microns. En 1 mm 3 – 200-400 mille.
Globules rouges matures – cellules anucléées, biconcaves. La partie principale est constituée de protéines contenant du fer hémoglobine. Transporte l'oxygène moléculaire, se transformant en un composé fragile - l'oxyhémoglobine. Le dioxyde de carbone est transporté des tissus par les globules rouges. Dans ce cas, l'hémoglobine est transformée en carbhémoglobine. En cas d'intoxication au monoxyde de carbone, un composé d'hémoglobine stable se forme - la carboxyhémoglobine, qui est incapable de lier l'oxygène.
des globules rouges se forment dans la moelle osseuse rouge des os plats à partir de cellules souches nucléaires. Les globules rouges matures circulent dans le sang pendant 100 à 120 jours, après quoi ils sont détruits dans la rate, le foie et la moelle osseuse. Les globules rouges peuvent également être détruits dans d’autres tissus (les bleus disparaissent).
Plaquettes– des cellules plates et anucléées de forme irrégulière qui participent au processus de coagulation sanguine et contribuent à la contraction des muscles lisses des vaisseaux sanguins. Formé dans la moelle osseuse rouge. Ils circulent dans le sang pendant 5 à 10 jours, puis sont détruits dans le foie, les poumons et la rate.
Leucocytes- des cellules nucléaires incolores qui ne contiennent pas d'hémoglobine. Le nombre de leucocytes peut fluctuer au cours de la journée en fonction de l'état fonctionnel de l'organisme. Les leucocytes remplissent une fonction phagocytaire.
Lymphocytes, un type de leucocytes, se forment dans les ganglions lymphatiques, les amygdales, l'appendice, la rate, le thymus et la moelle osseuse. Produire des anticorps et des antitoxines. Les anticorps protègent le corps des protéines étrangères - les antigènes.
La coagulation du sang – le mécanisme de protection le plus important qui protège le corps contre la perte de sang due à des dommages aux vaisseaux sanguins. Le processus de coagulation sanguine dépend d'un certain nombre de facteurs, dont les plus importants sont les ions Ca 2 + , déclenchant le processus de coagulation, prothrombine- une protéine du plasma sanguin qui est convertie en thrombine Et fibrinogène– protéine plasmatique soluble, transformée sous l'influence de la thrombine en protéine insoluble – fibrine. La fibrine dans l'air forme un caillot appelé thrombus.
Les médicaments contenant du chlorure de calcium et de la vitamine K contribuent à augmenter la capacité de coagulation du sang. En cas de pertes sanguines importantes, une transfusion sanguine est nécessaire.
Transfusion sanguine consiste à sélectionner le sang d'un donneur et à le transfuser au receveur.
Schéma de transfusion sanguine :
Lors d'une transfusion sanguine, il est nécessaire de prendre en compte la présence du facteur Rh.
La durée de vie des cellules sanguines est limitée. La relative constance de la quantité et de la composition du sang dans l'organisme est assurée, outre les vaisseaux sanguins, par les organes hématopoïétiques (moelle osseuse rouge, ganglions lymphatiques, rate, cellules hépatiques qui synthétisent les protéines plasmatiques) et les organes destructeurs du sang. (foie, rate).
Facteur Rh– une protéine présente dans le plasma sanguin de la plupart des gens. Ces personnes sont appelées groupes sanguins Rh-positifs. Les personnes Rh négatif n’ont pas cette protéine. Lors de la transfusion de sang, il est nécessaire de prendre en compte sa compatibilité avec le facteur Rh. Si une personne Rh négatif reçoit une transfusion de sang Rh positif, les globules rouges resteront collés les uns aux autres, ce qui peut entraîner la mort du receveur.
Immunité – assure la protection du corps contre les substances génétiquement étrangères et les infections. Prend en charge la spécificité corporelle.
Les réactions immunitaires sont assurées par les anticorps et les phagocytes. Les anticorps sont produits par les cellules dérivées des lymphocytes B en réponse à l'apparition d'antigènes dans l'organisme. L'antigène et l'anticorps forment un complexe antigène-anticorps dans lequel l'antigène perd ses propriétés pathogènes.
L'immunité innée associés aux anticorps reçus par l'enfant avec le lait maternel. De plus, elle est soutenue par la structure de la peau et des muqueuses, la présence d'enzymes bactéricides, l'environnement acide du suc gastrique, etc.
L'immunité acquise assurés par des mécanismes cellulaires et humoraux (la théorie de I. Mechnikov et P. Ehrlich). L'immunité qui apparaît après une maladie est dite naturelle. Si l’immunité apparaît après l’administration d’un vaccin contenant des agents pathogènes affaiblis ou leurs toxines, on parle d’immunité active artificielle. Après l'administration de sérum contenant des anticorps prêts à l'emploi, une immunité passive artificielle apparaît.
EXEMPLES DE TÂCHES
Partie A
A1. L'environnement interne du corps est constitué de
1) plasma sanguin, lymphe, substance intercellulaire
2) sang et lymphe
3) sang et substance intercellulaire
4) sang, lymphe, liquide tissulaire
A2. Le sang est constitué de
1) plasma et éléments formés
2) liquide intercellulaire et cellules
3) lymphe et éléments formés
4) éléments façonnés
A3. Un cal est une collection
A4. Les globules rouges remplissent la fonction
1) transport de l'oxygène 3) coagulation du sang
2) protection contre les infections 4) phagocytose
A5. La coagulation sanguine est associée à la transition
1) hémoglobine en oxyhémoglobine
2) thrombine en prothrombine
3) fibrinogène en fibrine
4) fibrine en fibrinogène
A6. Sang mal transfusé du donneur au receveur
1) empêche la coagulation du sang du receveur
2) n'affecte pas les fonctions corporelles
3) fluidifie le sang du receveur
4) détruit les cellules sanguines du receveur
A7. Personnes Rh négatif
3) sont des destinataires universels
4) sont des donneurs universels
A8. L'une des causes de l'anémie peut être
1) manque de fer dans les aliments
2) augmentation de la teneur en globules rouges dans le sang
3) la vie à la montagne
4) manque de sucre dans les aliments
A9. Les globules rouges et les plaquettes se forment
1) moelle osseuse jaune 3) foie
2) moelle osseuse rouge 4) rate
A10. Une augmentation des taux sanguins peut être le symptôme d’une maladie infectieuse.
1) érythrocytes 3) leucocytes
2) plaquettes 4) glucose
A11. L’immunité à long terme n’est pas développée contre
1) rougeole 3) grippe
2) varicelle 4) scarlatine
R12. Une victime d'une morsure de chien enragé est donnée
1) anticorps prêts à l'emploi
2) antibiotiques
3) agents pathogènes de la rage affaiblis
4) analgésiques
R13. Le danger du VIH est qu'il
1) provoque un rhume
2) conduit à une perte d’immunité
3) provoque des allergies
4) hérité
R14. Présentation du vaccin
1) conduit à la maladie
2) peut provoquer une forme bénigne de la maladie
3) guérit une maladie
4) ne conduit jamais à des problèmes de santé visibles
R15. La défense immunitaire de l'organisme est assurée
1) allergènes 3) anticorps
2) antigènes 4) antibiotiques
R16. L'immunité passive apparaît après l'administration
1) sérum 3) antibiotique
2) vaccins 4) sang de donneur
R17. L’immunité active acquise survient après
1) maladie antérieure 3) administration du vaccin
2) administration de sérum 4) naissance d'un enfant
R18. La spécificité interfère avec la greffe d'organes étrangers
1) glucides 3) protéines
2) lipides 4) acides aminés
R19. Le rôle principal des plaquettes est
1) défense immunitaire de l'organisme
2) transport de gaz
3) phagocytose des particules solides
4) la coagulation du sang
A20. Création de la théorie phagocytaire de l'immunité
1) L. Pasteur 3) I. Mechnikov
2) E. Jenner 4) I. Pavlov
Partie B
EN 1. Sélectionner les cellules sanguines et les substances qui assurent ses fonctions protectrices
1) globules rouges 3) plaquettes 5) hémoglobine
2) lymphocytes 4) fibrine 6) glucose
À 2 HEURES. Établir une correspondance entre le type d'immunité et ses caractéristiques
C1. Pourquoi un vaccin administré contre une maladie infectieuse ne protège-t-il pas une personne contre une autre maladie infectieuse ?
C2. Pour prévenir le tétanos, une personne en bonne santé a reçu du sérum antitétanique. Les médecins ont-ils fait le bon choix ? Prouvez votre réponse.
Extrait du livre Tout sur tout. Volume 1 auteur Likoum ArkadyQu'est-ce qu'une transfusion sanguine ? Le besoin de sang peut survenir pour de nombreuses raisons : un soldat a été blessé, un ouvrier d'usine a eu un accident, une personne est sur le point de mourir à cause d'une hémorragie interne, un patient affaibli a besoin de soins sérieux.
Extrait du livre Savoir comment prodiguer les premiers secours auteur Maslinkovsky T I Extrait du livre Grande Encyclopédie Soviétique (GR) de l'auteur BST Extrait du livre Grande Encyclopédie Soviétique (PE) de l'auteur BST Extrait du livre Biologie [Ouvert de référence complet pour la préparation à l'examen d'État unifié] auteur Lerner Georgy Isaakovich5.3. Environnement interne du corps humain. Groupes sanguins. Transfusion sanguine. Immunité. Métabolisme et conversion d'énergie dans le corps humain. Vitamines 5.3.1. Environnement interne du corps. Composition et fonctions du sang. Groupes sanguins. Transfusion sanguine. Immunité Termes de base et
Extrait du livre Guide de poche des tests médicaux auteur Rudnitski Léonid Vitalievitch2. Groupes sanguins Depuis des temps immémoriaux, les hommes savent que le sang est porteur de vie. L’homme ancien, chasseur et guerrier, observait comment la vie de la personne ou de l’animal qu’il avait vaincu s’éteignait à mesure que le sang se perdait. On croyait qu'avec l'aide de sang frais, il était possible
Extrait du livre Manuel de diagnostic de l'immunologiste auteur Polushkina Nadejda NikolaevnaPartie V Groupes sanguins humains et santé
Extrait du livre Les bizarreries de notre évolution par Harrison KeithChapitre 1 Les groupes sanguins comme facteur immunologique Il existe 4 groupes sanguins humains : 0 (I), A (II), B (III) et AB (IV). Les groupes sanguins sont le résultat d’une longue évolution du système immunitaire, au cours de laquelle s’est effectuée une adaptation à des conditions naturelles et climatiques en constante évolution.
Extrait du livre Des criminels particulièrement dangereux [Crimes qui ont secoué le monde] auteur Globus Nina VladimirovnaChapitre 2 Groupes sanguins et réactions à la vaccination Une légère introduction d'un vaccin dans l'organisme peut avoir des effets non seulement positifs, mais également négatifs. Cela est dû aux caractéristiques individuelles du corps, notamment au groupe sanguin. Groupe sanguin 0 (I)
Extrait du livre Comment élever un enfant en bonne santé et intelligent. Votre bébé de A à Z auteur Shalaeva Galina PetrovnaChapitre 3 Groupes sanguins et plantes médicinales Lors d'un traitement avec des plantes médicinales, il est important de considérer le groupe sanguin du patient (Tableau 54). Ainsi, les personnes des groupes sanguins 0 (I), B (III) et AB (IV) excluent les plats de viande de leur alimentation, et celles des groupes B (III) et AB (IV) ne le font pas.
Extrait du livre ABC de la santé des enfants auteur Shalaeva Galina PetrovnaChapitre 1 Détermination du groupe sanguin selon le système des facteurs avo et Rh Détermination du groupe sanguin La détermination est réalisée à l'aide de sérums standards, la méthode est basée sur la réaction de l'agglutinine et des globules rouges du patient avec du sérum contenant certains anticorps.
Extrait du livre Comment prendre soin de soi si on a plus de 40 ans. Santé, beauté, minceur, énergie auteur Karpoukhina Victoria VladimirovnaGroupes sanguins Les globules rouges possèdent à leur surface des molécules appelées antigènes. Il en existe deux types : A et B. Nous héritons de ces types de nos parents et ils déterminent notre groupe sanguin. Le système AB0 est utilisé pour désigner les groupes sanguins. Parfois
Extrait du livre de l'auteurFORMATION DANS LE SANG Ce crime meurtrier s'est produit à l'aube du siècle - en décembre 1901. Toute la Russie parlait de lui avec colère. Les gens se demandaient : d’où viennent ces tueurs dégénérés et cruels ? Malheureusement, à ce jour, personne n’a donné de réponse intelligible à cette question.
951 0
Pour conclure la discussion sur les possibilités du potentiel cytotoxique de diverses cellules du corps, nous ne pouvons ignorer un autre type de cellule.
Nous parlons de plaquettes - des cellules qui, selon les concepts généralement acceptés, ne sont pas considérées aujourd'hui comme des cellules du système immunitaire.
Cependant, ils ont une activité cytotoxique contre diverses cellules tumorales, mais leur capacité à lyser les cellules cibles a été la moins étudiée.
L’intérêt porté à l’étude du rôle des plaquettes dans le processus tumoral n’est pas seulement dû à leur participation à la lyse des cibles tumorales ; il peut être discuté sous au moins plusieurs aspects.
Le premier est un effet cytotoxique contre diverses tumeurs, le second est la participation à la mise en œuvre des fonctions de cellules du système immunitaire telles que cellules tueuses naturelles (NK), les monocytes, certains lymphocytes T (prolifération, migration, adhésion, etc.), et le troisième est l'interaction des plaquettes avec les cellules tumorales.
Du point de vue des idées déjà formées, le dernier aspect n'est pas directement lié à la protection immunologique antitumorale, mais il est important pour comprendre les caractéristiques du microenvironnement et, par conséquent, pour la mise en œuvre des fonctions des cellules du système immunitaire.
Sans s'attarder sur les propriétés générales et assez connues des plaquettes, il semble opportun de s'intéresser à celles qui sont importantes au regard de la problématique abordée.
Récemment, de nombreuses informations sont apparues sur l'expression de diverses structures par les plaquettes, de plus en plus nombreuses. Pour comprendre le rôle des plaquettes dans le processus tumoral, l’expression des structures suivantes revêt une importance particulière.
Tout d’abord, il convient de souligner que les plaquettes possèdent de nombreuses molécules qui leur offrent de nombreuses possibilités d’adhésion. Diverses intégrines jouent un rôle important dans les propriétés adhésives des plaquettes, en particulier la chaîne d'intégrine β1, une glycoprotéine transmembranaire (CD29), capable de se lier à VICAM-1 et MAaCAM-1 et de former des hétérodimères avec la fibronectine, la laminine et le collagène β1. chaîne.
Non moins important est le rôle du CD41 - glycoprotéine lib (GPIIb), qui est la sous-unité a du complexe CD41-CD61 - un hétérodimère dépendant du calcium ; Une particularité de l'expression de CD41, ainsi que de CD42a, CD42b, CD42c, est qu'ils apparaissent exclusivement sur les plaquettes et les mégacaryocytes. Les propriétés adhésives des plaquettes sont également associées à l'expression de la molécule d'adhésion intercellulaire - ICAM-2 (CD102), ainsi qu'à la molécule d'adhésion potentielle - CD147.
Une place importante dans les propriétés adhésives des plaquettes est occupée par la P-sélectine (CD62), une protéine liée à la membrane des plaquettes et des cellules endothéliales, qui est mobilisée sous l'influence de médiateurs (histamine, composants du complément, etc.) ; ses ligands sont les molécules sialyl-Lewis X et sialyl-Lewis A.
L’expression du récepteur du facteur de croissance dérivé des plaquettes (CD140a), impliqué dans la prolifération et la migration de ces cellules, joue un rôle important dans le fonctionnement des plaquettes. Le rôle de l'expression du récepteur Fc des IgE n'est pas moins important.
Certaines structures de surface exprimées par les plaquettes sont directement liées à la régulation des fonctions cellulaires du système immunitaire. Les plaquettes possèdent à leur surface une glycoprotéine membranaire qui participe à l’adhésion des thymocytes et des cellules épithéliales thymiques.
Une molécule telle que CD226, une glycoprotéine, est exprimée non seulement par les plaquettes, mais aussi par les cellules NK, les monocytes et certains lymphocytes T, participant à l'adhésion des lymphocytes T à d'autres cellules possédant le ligand correspondant.
Les antigènes courants exprimés par les plaquettes et certaines cellules du système immunitaire comprennent l'antigène CD245 d'un poids moléculaire de 220 à 240 kDa, qui est également exprimé par les monocytes, les lymphocytes et les granulocytes et est impliqué dans la transmission du signal et la co-stimulation des lymphocytes T. et des cellules tueuses naturelles.
Enfin, il convient de noter que CD36 fait partie de la famille des récepteurs scavenger, impliqués dans l'interaction des plaquettes avec les monocytes et les cellules tumorales, la reconnaissance et la phagocytose.
Les plaquettes expriment également le CD114, une molécule transmembranaire de type I (membre de la famille des récepteurs de cytokines de type I), impliquée dans la régulation des fonctions et la prolifération des cellules lymphoïdes.
Les plaquettes ont un grand potentiel d'interaction avec le collagène, les récepteurs qu'elles expriment, ce qui facilite leur interaction avec la matrice extracellulaire, constituée principalement de collagène de types I, II et III ; Ce processus implique la glycoprotéine plaquettaire lb et le FVIII/vWF, ce dernier étant nécessaire à la fixation à l'endothélium. Les plaquettes expriment l'antigène HPA-1a.
Il est également très significatif que les plaquettes agissent comme messager secondaire sous l'action de l'histamine et du cytochrome P450.
Les plaquettes sont capables d'exercer certaines influences régulatrices sur de nombreuses cellules du système immunitaire (lymphocytes T, diverses cellules présentatrices d'antigènes, etc.). Cet effet est principalement dû aux effets des produits granulés plaquettaires, ainsi qu'au facteur plaquettaire 4 (PF4) qu'ils produisent, RANTES, une forme soluble du CD40L.
Les données sur les caractéristiques des plaquettes, qui sont loin d'être présentées dans leur intégralité, ne laissent néanmoins aucun doute sur le fait qu'elles peuvent être impliquées dans divers processus qui dépassent largement le concept de ces cellules.
Dans le tableau 11 montre les caractéristiques générales des plaquettes.
Tableau 11. Caractéristiques générales des plaquettes
Effet cytotoxique des plaquettes
La cytotoxicité des plaquettes, comme les éosinophiles et les basophiles, a été observée pour la première fois lors de la lyse des schistosomes. De plus, le transfert passif de plaquettes provenant de rats immunisés avec Schistosoma mansoni s'est avéré les protéger d'une infection ultérieure.Compte tenu du rôle des plaquettes dans l'effet anthelminthique, les auteurs l'ont évalué comme auxiliaire de la cytotoxicité des phagocytes mononucléés, ainsi que des mastocytes, et ont noté que le facteur induisant la cytotoxicité plaquettaire est le récepteur Fc des IgE.
Les mêmes chercheurs ont montré plus tard que, outre le récepteur de faible affinité pour les IgE (FceRII), ils expriment également un récepteur de haute affinité pour cet isotype d'immunoglobulines - FceRI ; l'expression de ces derniers est très hétérogène et seul un petit nombre de plaquettes co-expriment les deux récepteurs.
La cytotoxicité plaquettaire peut être induite par différents stimulants (ionopores calciques, PAF, PHA, ricine…). Tous les facteurs améliorent la production de thromboxane-2 par les plaquettes et l'hydrolyse des produits du thromboxane A ; vis-à-vis des cellules de certaines lignées tumorales, notamment K562, la cytotoxicité plaquettaire s'accompagnait d'une activation des deux facteurs.
Actuellement, deux mécanismes principaux de cytotoxicité plaquettaire sont connus : l'action des produits de la cyclooxygénase (TXA2/PGH2) et de l'oxyde nitrique.
Les cellules tumorales se distinguent par une sensibilité différente à l'action lytique des plaquettes, ce qui est confirmé par les données d'études de cellules de différentes lignées : les cellules des lignées K562, KU812, LU99A, KG1 étaient sensibles, et les cellules des lignées U937, M1APaCa2 et MOLT -4 lignes étaient totalement insensibles.
En particulier, une étude de la cytotoxicité des plaquettes contre les lignées cellulaires K562 et LU99A (cancer du poumon) a montré qu'elles présentaient une sensibilité différente aux produits plaquettaires cytotoxiques (divers inhibiteurs de la cyclooxygénase et de l'oxyde nitrique ont été utilisés) : si les cellules de la lignée K.562 étaient lysées avec la participation de produits cyclooxygénases, les cellules de la lignée LU99A sont alors sous l'influence du monoxyde d'azote.
En plus de ces différences dans la sensibilité des cellules tumorales individuelles, il existe également des différences dans l'action des plaquettes activées et non activées, ce qui a été confirmé par des études au microscope électronique. Il s’est avéré que les plaquettes non stimulées s’attachent aux cellules K562, mais pas celles stimulées.
Il s'ensuit que sans stimulation des plaquettes, un contact direct entre elles et les cellules tumorales est obligatoire, mais pour les plaquettes stimulées, ce n'est pas nécessaire. On suppose également que l’effet de la lyse des plaquettes est associé à leurs facteurs solubles, qui sont facilement inactivés.
Les faits ci-dessus confirment encore davantage l'universalité de l'importance des propriétés biologiques des cellules tumorales pour toute forme de leur interaction avec diverses cellules.
La variété des cellules des différentes lignées tumorales étudiées par les auteurs leur a permis de conclure que les plaquettes sont des cellules cytotoxiques effectrices dans la défense antitumorale.
Enfin, comme indiqué précédemment, les plaquettes peuvent avoir des effets régulateurs sur les monocytes, les lymphocytes NK et T, modifiant ainsi leur effet cytotoxique. Malgré le fait que cette question ait été très peu étudiée, la validité de sa formulation est confirmée par les données selon lesquelles la présence de plaquettes augmente dans certains cas la cytotoxicité des monocytes.
Les principaux mécanismes de cytotoxicité plaquettaire sont présentés dans la Fig. 53.

Riz. 53. Mécanismes de cytotoxicité plaquettaire
Ainsi, à partir des quelques données présentées, il devient évident que les plaquettes ont également la capacité d'avoir un effet cytotoxique contre diverses cibles tumorales, mais les mécanismes de cette action font l'objet d'études plus approfondies.
Effet négatif des plaquettes sur la croissance tumorale
Outre leur capacité à avoir un effet cytotoxique, les plaquettes peuvent également affecter négativement la protection antitumorale. Malgré le fait que la participation de diverses cellules à l'immunostimulation de la croissance fera l'objet d'une discussion dans la troisième partie de la monographie, il a semblé opportun d'aborder ici la question de l'effet négatif des plaquettes, car, premièrement, elles ne sont pas classiques. cellules du système immunitaire, et deuxièmement, les données sur elles ne sont pas directement impliquées dans l'immunostimulation.On sait que les plaquettes infiltrent souvent le tissu tumoral, ce qui soulève la question : comment leur présence affecte-t-elle l'action du TNFa, l'un des composants importants de la cytotoxicité ?
Pour répondre à cette question, la lignée cellulaire de fibrosarcome L929 a été exposée aux plaquettes et il a été démontré que la présence de plaquettes affaiblit la cytolyse dépendante du TNFa. Cependant, l’absence d’effet du TNFa n’était associée ni à sa dégradation ni à la perte de la capacité des cellules tumorales à se lier à ce facteur. Il s’est avéré que le TNFa interagit avec certaines zones des plaquettes, entraînant une liaison incomplète aux cellules tumorales.
Le rôle négatif des plaquettes inclut également le fait que, dans certaines conditions, elles protègent les cellules tumorales de la lyse des cellules tueuses naturelles in vitro et in vivo. Dans des expériences avec des cellules de différentes lignées (CFS1, B16), il a été démontré que l'agrégation plaquettaire autour des cellules tumorales inhibe leur lyse par NK.
L'utilisation de lignées cellulaires à la fois sensibles et insensibles aux cellules tueuses naturelles a montré que dans tous les cas, les plaquettes favorisent la survie des cellules tumorales dans le sang périphérique, améliorant ainsi le processus de métastases.
La confirmation que les plaquettes interfèrent avec la mise en œuvre de l'effet NK sont des expériences avec des cellules de mélanome non métastatiques de la lignée SBcl2 et l'utilisation d'éritostatine, qui se lie à l'intégrine αIIβ3 : sous l'influence de ce médicament, les cellules de mélanome sont devenues très sensibles aux NK-like. Cellules TALL-104 ; le récepteur avec lequel l'éritostatine interagit avec les cellules de mélanome est inconnu.
La capacité des plaquettes à interagir avec les cellules tumorales est particulièrement intéressante. Cette capacité et sa gravité dépendent en grande partie des caractéristiques biologiques de la cellule tumorale. L’une des manifestations importantes de cette interaction est l’agrégation plaquettaire, associée à l’apparition de métastases.
Ces données ont été obtenues sur des lignées cellulaires de diverses tumeurs ; Il a été démontré que l'interaction de la tumeur et des plaquettes favorise activement l'agrégation de ces dernières dans le fibrosarcome hautement métastatique RAC 17.15 (cet effet par rapport à la tumeur faiblement métastatique RAC 17.14 est faiblement exprimé).
Lors de l'étude des cellules de mélanome et d'adénosarcome M7609, il a été constaté qu'elles provoquent une agrégation plaquettaire dans le plasma hépariné ; dans certains cas, ce processus dépend de la participation de la glycoprotéine membranaire GPlb, dans d'autres - de la glycoprotéine GPIb/IIIa.
Les plaquettes sont également activées par les cellules du carcinome pulmonaire à petites cellules et du neuroblastome, un processus médié par la sélectine P en se liant aux structures glucidiques contenant des molécules sialyl-Lewis. La présence de la chaîne glucidique sialysée de la gp44 favorise également l'agrégation des cellules d'adénocarcinome de souris (ligne 26).
Une étude de divers sous-types histologiques de lignées cellulaires de cancer du poumon humain (carcinome à petites cellules, carcinome épidermoïde, à grandes cellules, adénocarcinome et carcinome à cellules alvéolaires) a montré que les cellules des lignées répertoriées utilisent différentes voies d'activation plaquettaire : pour certaines cellules, l'agrégation est associé à la présence de facteurs de coagulation VII et X, pour d'autres - à la nécessité d'un contact direct entre la tumeur et les plaquettes.
Très souvent, l’interaction entre les cellules tumorales et les plaquettes est également combinée à une interaction avec les cellules endothéliales et la matrice extracellulaire. Une place importante dans l'interaction entre les cellules tumorales, les plaquettes et la matrice extracellulaire est occupée par la glycoprotéine GPIIb/IIIa du côté des plaquettes, et les intégrines a(v) du côté de la tumeur, comme le montre l'étude de trois lignées. de mélanome humain et une lignée de carcinome.
En figue. 54 illustre une agrégation accrue des plaquettes lors de leur interaction avec les cellules tumorales.

Riz. 54. Agrégation plaquettaire lors de l'interaction avec les cellules tumorales
Dans certains cas, les plaquettes présentes dans les systèmes in vitro peuvent empêcher l’adhésion de la tumeur aux cellules endothéliales. Cependant, l'élimination des plaquettes in vivo s'accompagnait d'une inhibition des métastases, comme le montrent les modèles de croissance tumorale induite par des cellules de diverses lignées de souris (cellules épithéliales) et des cellules tumorales telles que les cellules de fibrosarcome et de thymome.
Il n'a pas été possible de clarifier le rôle de diverses molécules d'adhésion (ICAM-1, LTA-1, VCAM-1, E- et P-sélectines) utilisant leur modificateur sur le développement des métastases.
De nombreux autres faits pourraient être cités pour illustrer la participation des plaquettes à l’amélioration des métastases. Cependant, indépendamment de cela, les propriétés biologiques des plaquettes indiquent leur capacité prononcée à interagir activement avec les cellules tumorales et endothéliales, ainsi qu'avec la matrice extracellulaire. Le résultat de cette interaction peut être plusieurs mécanismes d’augmentation des métastases impliquant les plaquettes.
Ces mécanismes comprennent principalement :
1) la possibilité de stimuler la prolifération des cellules tumorales ;
2) renforcer l'interaction des cellules tumorales avec la matrice extracellulaire ;
3) migration accrue des cellules tumorales dans le lit vasculaire.
Ces faits incontestables suffisent déjà à reconnaître la validité du traitement anticoagulant, qui réduit le risque de propagation des métastases en influençant les plaquettes. Il y a tout lieu de croire qu'élargir la gamme des études immunologiques prenant en compte le rôle des plaquettes pourrait être une direction assez prometteuse en onco-immunologie.
Berezhnaya N.M., Chekhun V.F.
Immunité- la capacité de l'organisme à reconnaître l'invasion de matières étrangères et à mobiliser les cellules et les substances qu'elles produisent pour éliminer plus rapidement et plus efficacement ces matières.
Frank Burnett, prix Nobel de physiologie ou médecine.
Glossaire des termes de base
Immunité– la capacité de l’organisme à se protéger des bactéries, virus, corps étrangers, à s’en débarrasser et ainsi à maintenir la constance de l’environnement interne de l’organisme.
Phagocytose– le processus de « déglutition » des micro-organismes par les leucocytes, ainsi que des restes de cellules mortes et d'autres particules, par exemple la poussière dans les poumons.
Phagocytes– certains leucocytes qui effectuent le processus de phagocytose. Les phagocytes sont capables de mouvements amiboïdes en raison de la formation de pseudopodes.
Anticorps– protéines produites par les lymphocytes B en réponse à la présence d'une substance étrangère – antigène. Les anticorps sont strictement spécifiques. Le corps humain est capable de produire environ 100 millions d’anticorps différents qui reconnaissent presque toutes les substances étrangères.
Antigène– une molécule étrangère qui provoque la formation d’anticorps. Les antigènes peuvent être des microbes, des virus ou toute cellule dont la composition diffère de celle des propres cellules de l’organisme.
Antitoxine– une substance protectrice spéciale. Les antitoxines neutralisent les poisons microbiens circulant dans le sang.
Vaccin– un médicament contenant des agents pathogènes tués ou affaiblis, c'est-à-dire un médicament contenant une petite quantité d’antigènes.
Sérum cicatrisant– une préparation contenant des anticorps prêts à l’emploi. Le sérum est préparé à partir du sang d'animaux préalablement spécifiquement infectés par l'agent causal de la maladie. Parfois, le sérum est préparé à partir du sang d’une personne qui a eu une maladie, comme la grippe.
Macrophages– de grosses cellules capables de phagocytose, situées dans les tissus. Effectuer des fonctions sanitaires et de protection.
Organes du système immunitaire
1. Thymus(glande thymus) est située derrière le sternum. Fonctionne uniquement chez les enfants. Joue un rôle important dans le développement du système immunitaire. Les lymphocytes T se forment et mûrissent dans le thymus.
2. Moelle trouvé dans les os tubulaires. Des cellules sanguines s'y forment - globules rouges, leucocytes, plaquettes, macrophages. Les lymphocytes nés ici migrent vers le thymus. En y mûrissant, ils forment des lymphocytes T.
3. Ganglions lymphatiques– les ganglions situés le long des vaisseaux lymphatiques. Ils contiennent des lymphocytes. Ils filtrent la lymphe et la débarrassent des virus, des bactéries et des cellules cancéreuses.
4. Rate– un organe dans lequel se forment les lymphocytes. Il s'agit d'un filtre biologique : il élimine les cellules sanguines vieillies et endommagées, dissout et absorbe les bactéries et autres substances étrangères. Agit comme un dépôt de sang.
La résistance non spécifique est fournie par :
1. Imperméabilité de la peau et des muqueuses saines aux micro-organismes ;
2. La présence d'organes protecteurs : foie, ganglions lymphatiques, rate ;
3. La présence de substances bactéricides dans les liquides : salive, larmes, sang, lymphe, liquide tissulaire.
4. Les sécrétions des glandes sudoripares et sébacées, ainsi que l'acide chlorhydrique, protègent contre les micro-organismes.
Notre corps dispose de plusieurs formes de protection contre les corps et composés étrangers.
Immunité non spécifique– la forme d’immunité la plus ancienne, réalisée par les leucocytes par phagocytose. Immunité spécifique est la capacité du corps à reconnaître des substances autres que ses cellules et ses tissus et à détruire uniquement ces antigènes.
Rappelons qui sont les lymphocytes. Ces cellules représentent 20 à 40 % des globules blancs. Les lymphocytes, contrairement à tous les autres leucocytes, sont capables non seulement de pénétrer dans les tissus, mais également de retourner dans le sang. Les lymphocytes représentent le maillon central du système immunitaire de l'organisme.
Il existe deux types de lymphocytes dans le corps : les lymphocytes T et les lymphocytes B.
Les lymphocytes T naissent dans la moelle osseuse, mûrissent dans le thymus puis s'installent dans les ganglions lymphatiques, la rate ou le sang, où ils représentent 40 à 70 % de tous les lymphocytes. Les lymphocytes T sont capables de reconnaître les antigènes.
Les lymphocytes B se forment dans la moelle osseuse et mûrissent dans le tissu lymphoïde de l'appendice et des amygdales. Les lymphocytes B, ayant reçu des informations sur l'antigène du lymphocyte T, commencent à se multiplier rapidement et à synthétiser des anticorps.
Mécanismes cellulaires et humoraux de l'immunité
Immunité cellulaire: Les lymphocytes T reconnaissent les micro-organismes, les virus, les organes et tissus transplantés et les cellules malignes. La cellule immunitaire entière participe à la réaction ; les anticorps libres ne sont pas libérés.
Immunité humorale: Les lymphocytes B libèrent des anticorps dans le plasma sanguin, le liquide tissulaire et la lymphe. Certains anticorps collent les micro-organismes entre eux, d’autres précipitent les particules collées et d’autres encore les détruisent et les dissolvent.
Types d'immunité :
| Naturel | Artificiel | |
| Passif | Les anticorps maternels pénètrent dans le placenta et pénètrent dans le sang fœtal et protègent le bébé. Dans les premiers jours de sa vie, le bébé reçoit des anticorps par le lait, qui sont absorbés dans les intestins sans dégradation. | L’administration d’anticorps assure une protection immédiate contre l’infection, mais cette protection ne dure pas longtemps car le nombre d’anticorps diminue progressivement. |
| Actif | Le corps produit ses propres anticorps à la suite d’une infection. La rougeole, la varicelle, la coqueluche et les oreillons laissent généralement une immunité durable. | L'introduction de vaccins provoque l'apparition d'anticorps dans le plasma de la personne vaccinée. Actuellement, des techniques ont été développées pour créer des anticorps à l’aide de méthodes biotechnologiques modernes. |
Processus inflammatoire.
Lorsqu'une zone du corps est blessée, une réaction locale se produit, se manifestant par un gonflement et une douleur. Cette condition est appelée inflammation. L'inflammation s'accompagne des symptômes suivants :
1. Une expansion locale des capillaires se produit, entraînant une augmentation du flux sanguin vers cette zone. Des rougeurs et de la fièvre apparaissent.
2. En raison de la perméabilité capillaire accrue, le plasma et les leucocytes s'échappent dans les tissus environnants. Un gonflement se produit.
3. Les leucocytes sont envoyés aux bactéries, une phagocytose se produit. Si un phagocyte absorbe plus de microbes qu’il ne peut en digérer, il meurt. Un mélange de phagocytes et de bactéries morts et vivants est appelé pus.
4. Les symptômes émergents entraînent une irritation des récepteurs, provoquant une sensation de douleur.
Plan
1. Introduction
2.Formes d’immunité :
a) immunité naturelle ;
b) immunité acquise.
3.Mécanismes d'immunité
4.Inflammation et phagocytose
5.Régulation de l'immunité
6. Fonction barrière de l’immunité
7.Réactivité immunologique
8.Pathologie de l'immunité
a) l'origine du virus de l'immunodéficience ;
b) Comment peut-on être infecté par le SIDA ?
c) Le SIDA ne peut pas être contracté par...
10.Littérature
Introduction
Immunité- l'immunité de l'organisme face à un agent infectieux ou à toute substance étrangère.
L'immunité est déterminée par l'ensemble de toutes ces adaptations héréditaires et individuellement acquises par l'organisme qui empêchent la pénétration et la reproduction des microbes, virus et autres agents pathogènes et l'action des produits qu'ils sécrètent. La protection immunologique ne peut pas viser uniquement les agents pathogènes et les produits qu'ils sécrètent. Toute substance qui est un antigène, par exemple une protéine étrangère à l'organisme, provoque des réactions immunologiques à l'aide desquelles cette substance est en quelque sorte éliminée de l'organisme.
L'évolution a façonné le système immunitaire depuis environ 500 millions d'années. Ce chef-d'œuvre de la nature nous ravit par la beauté de l'harmonie et de la détermination. La curiosité persistante des scientifiques de diverses spécialités nous a révélé les lois de son fonctionnement et a donné naissance à la science de « l’immunologie médicale » au cours des 110 dernières années.
Chaque année apporte son lot de découvertes dans ce domaine de la médecine en développement rapide.
Antigènes – substances perçues par l'organisme comme étrangères et provoquant une réponse immunitaire spécifique. Capable d'interagir avec les cellules du système immunitaire et les anticorps. L'entrée d'antigènes dans l'organisme peut conduire à la formation d'une immunité, d'une tolérance immunologique ou d'allergies. Les protéines et autres macromolécules ont les propriétés des antigènes. Le terme « antigène » est également utilisé en relation avec les bactéries, les virus et les organes entiers (lors d'une transplantation) contenant l'antigène. La détermination de la nature de l'antigène est utilisée dans le diagnostic des maladies infectieuses, lors de transfusions sanguines, de transplantations d'organes et de tissus. Les antigènes sont également utilisés pour créer des vaccins et des sérums.
Anticorps - protéines (immunoglobulines) présentes dans le plasma sanguin des humains et des animaux à sang chaud, formées lorsque divers antigènes pénètrent dans l'organisme et sont capables de se lier spécifiquement à ces antigènes. Ils protègent l'organisme des maladies infectieuses : en interagissant avec les micro-organismes, ils empêchent leur reproduction ou neutralisent les imitoxines libérées.
Tous les agents pathogènes et substances de nature antigénique perturbent la constance de l'environnement interne de l'organisme. Pour équilibrer ce trouble, le corps utilise l'ensemble de ses mécanismes visant à maintenir un environnement interne constant. Les mécanismes immunologiques font partie de ce complexe. Immunisé est l'organisme dont les mécanismes soit ne permettent pas du tout de violer la constance de son environnement interne, soit permettent d'éliminer rapidement cette violation. Ainsi, l'immunité est un état d'immunité provoqué par un ensemble de processus visant à restaurer la constance de l'environnement interne de l'organisme, perturbé par des agents pathogènes et des substances à caractère antigénique.
L'immunité de l'organisme contre les infections peut être due non seulement à sa réactivité immunologique, mais également à d'autres mécanismes. Par exemple, l'acidité du suc gastrique peut protéger contre l'infection par la bouche par certaines bactéries, et un organisme avec plus d'acidité du suc gastrique en est plus protégé qu'un organisme avec moins d'acidité. Dans les cas où la protection n’est pas due à un mécanisme immunologique, on dit que l’organisme présente une résistance. Il n’est pas toujours possible de tracer une ligne claire entre immunité et résistance. Par exemple, les modifications de la résistance de l'organisme aux infections qui surviennent à la suite de la fatigue ou du refroidissement sont davantage déterminées par des modifications des constantes physiologiques de l'organisme que par des facteurs de défense immunologiques. Cette ligne est plus nette dans les phénomènes d'immunité acquise, caractérisés par une spécificité élevée, absente dans les phénomènes de résistance.
Formes d'immunité
L'immunité est diverse dans son origine, sa manifestation, son mécanisme et un certain nombre d'autres caractéristiques, grâce auxquelles il existe une classification de divers phénomènes immunologiques sous la forme de certaines formes d'immunité. Par origine
Une distinction est faite entre l’immunité naturelle, innée et acquise.
Immunité naturelle- l'immunité due à des caractéristiques biologiques innées inhérentes à une espèce animale ou humaine donnée. Il s’agit d’une caractéristique d’espèce héritée, comme toute autre caractéristique morphologique ou biologique d’une espèce. Des exemples de cette forme d’immunité incluent l’immunité des humains contre la maladie de Carré ou de nombreux animaux contre la rougeole. On l'observe à la fois chez le même animal pour de nombreux agents infectieux, par exemple chez les bovins pour la maladie de Carré, la maladie de Carré et la grippe aviaire, et chez différents animaux pour le même agent infectieux (par exemple, tous les animaux sont immunisés contre le gonocoque).
La tension de l’immunité naturelle est très élevée. Elle est généralement considérée comme absolue, car dans l'écrasante majorité des cas, l'immunité naturelle ne peut pas être perturbée par une infection, même avec d'énormes quantités de matériel totalement virulent. Mais de nombreuses exceptions sont également connues, démontrant la relativité de l’immunité naturelle. Ainsi, il est possible d'infecter un poulet avec le charbon si sa température corporelle est artificiellement abaissée (normalement 41-420) à une température optimale pour le développement du microbe du charbon (370). Vous pouvez également infecter une grenouille naturellement immunisée contre le tétanos en augmentant artificiellement sa température corporelle. L'immunité naturelle peut dans certains cas être réduite par l'action des rayonnements ionisants et la création d'une tolérance immunologique. Dans certains cas, l’absence de maladie n’indique pas l’absence d’infection. La doctrine de l’infection latente permet de distinguer l’immunité contre une maladie de l’immunité contre un microbe. Dans certains cas, la maladie ne se produit pas du fait que le microbe entré dans le corps ne se multiplie pas et meurt ; dans d'autres cas, la maladie ne se produit pas, malgré le fait que le microbe ou le virus entré dans le corps s'y multiplie. Ces derniers cas, qui surviennent lors d'infections latentes d'organismes naturellement immunisés,
indiquent également la relativité de l’immunité naturelle. L'immunité naturelle est inhérente non seulement
organismes non sensibles. Les organismes sensibles possèdent également une certaine immunité, quoique faible, comme en témoigne le fait qu'un organisme sensible ne tombe malade qu'au contact d'une dose infectieuse de microbes. Si une dose plus faible pénètre dans le corps, ces microbes meurent et la maladie ne se produit pas. Par conséquent, un organisme sensible possède également un certain degré d’immunité naturelle. Cette « susceptibilité immunitaire naturelle » revêt une grande importance pratique. Une dose de microbes moins qu'infectieuse, sans provoquer de maladie, peut provoquer l'apparition d'une immunité acquise, indiquée par la formation d'anticorps. De la même manière, une vaccination progressive de la population par âge contre certaines infections se produit. Ces processus ont été bien étudiés dans la diphtérie.
Le nombre de réactions négatives de Schick augmente fortement avec l'âge, en raison du contact de la population avec le microbe diphtérique. La diphtérie survient dans un nombre beaucoup plus restreint de cas, et seule une petite proportion de personnes âgées (60 à 70 ans) qui ont de l'antitoxine dans le sang souffrent de diphtérie. Sans un certain degré d’immunité contre la diphtérie chez les jeunes enfants, n’importe quelle dose de bactérie diphtérique les rendrait malades, et il n’y aurait pas de vaccination liée à l’âge au sein de la population. Une situation similaire existe avec la rougeole, qui touche près de 100 % de la population. Avec la polio, il y a un changement dans l'autre sens : un petit nombre d'enfants tombent malades, mais presque toutes les personnes âgées de 20 à 25 ans possèdent des anticorps contre l'agent pathogène et ont donc été en contact avec celui-ci. Ainsi, la notion même de susceptibilité, synonyme de manque d’immunité, est relative. On ne peut parler de sensibilité qu'à certaines doses d'infection. En même temps, ce concept est purement physiologique, puisque la susceptibilité est déterminée précisément par l'appareil physiologique
un organisme né à la suite du processus évolutif.
L'immunité acquise est produite par l’organisme au cours de sa vie individuelle, soit par exposition à la maladie correspondante (immunité naturellement acquise), soit par vaccination (immunité acquise artificiellement). Il existe également une immunité acquise active et passive. L'immunité activement acquise se produit soit naturellement, lors d'une infection, soit artificiellement, lors d'une vaccination avec des microbes vivants ou morts ou leurs produits. Dans les deux cas, l’organisme qui acquiert l’immunité participe lui-même à sa création et produit un certain nombre de facteurs de protection appelés anticorps. Par exemple, après qu'une personne est infectée par le choléra, son sérum acquiert la capacité de tuer les microbes du choléra ; lorsqu'un cheval est immunisé avec la toxine diphtérique, son sérum acquiert la capacité de neutraliser cette toxine grâce à la formation d'une antitoxine dans le corps du cheval. . Si un sérum contenant une antitoxine déjà formée est administré à un animal ou à une personne qui n'a pas reçu la toxine auparavant, il est ainsi possible de reproduire une immunité passive due à une antitoxine qui n'a pas été produite activement par l'organisme qui a reçu le sérum, mais il y était passivement reçu avec le sérum administré.
L'immunité activement acquise, en particulier l'immunité acquise naturellement, qui s'établit des semaines après une maladie ou une vaccination, dure dans la plupart des cas longtemps - des années et des décennies ; parfois, elle persiste à vie (par exemple, immunité contre la rougeole). Cependant, il n’est pas hérité. Un certain nombre de travaux établissant la transmission héréditaire de l'immunité acquise n'ont pas été confirmés. Dans le même temps, la capacité de développer une immunité active est sans aucun doute une caractéristique spécifique inhérente à l'organisme, semblable à la susceptibilité ou à l'immunité naturelle. L'immunité acquise passivement s'établit très rapidement, généralement quelques heures après l'administration d'immunsérum, mais ne dure pas longtemps et disparaît au fur et à mesure que les anticorps introduits dans l'organisme disparaissent. Ce
survient le plus souvent en quelques semaines. L'immunité acquise sous toutes ses formes est le plus souvent relative et, malgré des tensions importantes, elle peut dans certains cas être vaincue par de fortes doses de matériel infecté, même si l'évolution de l'infection sera plus douce. L'immunité peut être dirigée soit contre les microbes, soit contre les microbes. les produits qu'ils forment, notamment les toxines ; Par conséquent, une distinction est faite entre l'immunité antimicrobienne, dans laquelle le microbe est privé de la possibilité de se développer dans le corps, ce qui le tue avec ses facteurs de protection, et l'immunité antitoxique, dans laquelle le microbe peut exister dans le corps, mais la maladie ne se produit pas, puisque l’organisme immunitaire neutralise les toxines du microbe.
Une forme particulière d’immunité acquise est ce qu’on appelle l’immunité infectieuse. Cette forme d’immunité n’est pas due à la transmission de l’infection, mais à sa présence dans l’organisme et n’existe que tant que l’organisme est infecté. Morgenroth (1920), qui a observé une forme ressemblant à celle de la souris chez des souris infectées par des streptocoques, l'a appelé immunité déprimée. Les souris infectées par de petites doses de streptocoque ne sont pas mortes, mais ont développé une infection chronique ; cependant, ils se sont révélés résistants à une infection supplémentaire par une dose mortelle de streptocoque, à partir de laquelle des souris témoins saines sont mortes. Une immunité de même nature se développe avec la tuberculose et certaines autres infections. L'immunité infectieuse est également appelée non stérile, c'est-à-dire elle ne libère pas le corps de l'infection, contrairement à d'autres formes d'immunité dites stériles, dans lesquelles le corps est libéré du principe infectieux. Cependant, une telle stérilisation n'a pas toujours lieu, car même en cas d'immunité acquise, le corps peut être porteur d'un microbe ou d'un virus pendant une longue période et, par conséquent, ne pas être « stérile » par rapport à l'infection.
La réactivité immunologique différente des tissus et organes individuels du corps et la divergence dans de nombreux cas entre la présence d'immunité et la présence d'anticorps ont servi de base à la construction de la théorie de l'immunité locale par A. M. Bezredki
(1925). Selon cette théorie, l’immunité locale se produit indépendamment de l’immunité générale et n’est pas associée aux anticorps. Seuls certains tissus sont sensibles à l'infection (par exemple, seule la peau est sensible au charbon) et donc leur immunisation entraîne une immunité générale de l'organisme. D'où la proposition d'immuniser la peau contre les infections cutanées, les intestins contre les infections intestinales. Une grande quantité de matériel expérimental obtenu dans l'étude de cette question a montré que l'immunité locale, en tant que phénomène dépendant de l'organisme tout entier, n'existe pas et que dans tous les cas, l'immunisation locale s'accompagne de l'émergence d'une immunité générale avec formation de anticorps. Dans le même temps, il a été constaté que l'immunisation locale peut être conseillée dans certains cas en raison des particularités de la réaction immunologique de certains tissus.
Mécanismes d'immunité
Les mécanismes de l'immunité peuvent être schématiquement répartis dans les groupes suivants : barrières cutanées et muqueuses ; inflammation, phagocytose, système réticuloendothélial, fonction barrière du tissu lymphatique ; facteurs humoraux ; réactivité des cellules du corps.
Barrières cutanées et muqueuses. La peau est impénétrable pour la plupart des bactéries : toutes les influences qui augmentent la perméabilité cutanée réduisent sa résistance aux infections, et toutes les influences qui réduisent sa perméabilité agissent dans la direction opposée. Cependant, la peau n’est pas seulement une barrière mécanique pour les microbes. Il possède également des propriétés stérilisantes et les microbes qui pénètrent dans la peau meurent rapidement. Arnold (1930) et d'autres scientifiques ont observé que le bâtonnet miraculeux placé sur une peau humaine saine disparaît si rapidement qu'après 10 minutes, seulement 10 % et après 20 minutes - 1 % de la quantité totale de bactéries placées sur la peau peuvent être détectées. ; Après 30 minutes, la baguette miraculeuse n'était plus du tout détectable. Les bacilles intestinaux et typhoïdes ont disparu au bout de 10 minutes. Il a été établi que l’effet bactéricide de la peau est lié à son degré de propreté. L'effet stérilisant de la peau ne se retrouve que par rapport aux types de microbes qui entrent en contact avec elle relativement rarement ou n'entrent pas du tout en contact avec elle. Elle est négligeable par rapport aux microbes qui habitent fréquemment la peau, comme la jaunisse du staphylocoque. Il y a des raisons de croire que les propriétés bactéricides de la peau sont principalement dues à la teneur en acides lactiques et gras des sécrétions de la sueur et glandes sébacées. Il a été démontré que les extraits alcooliques éthérés de la peau contenant des acides gras et des savons ont un effet bactéricide notable contre les streptocoques, les bacilles diphtériques et les bactéries intestinales, tandis que les extraits salés sont dépourvus ou presque dépourvus de cette propriété.
Les muqueuses constituent également la barrière protectrice de l'organisme contre les microbes, et cette protection n'est pas due uniquement à des fonctions mécaniques. La forte acidité du suc gastrique, ainsi que la présence de salive, qui possède des propriétés bactéricides, empêchent la prolifération des bactéries. . La muqueuse intestinale, qui contient un grand nombre de bactéries, possède des propriétés bactéricides prononcées. L'effet bactéricide des écoulements muqueux est également associé à la présence d'une substance spéciale dans ces écoulements - le lysozyme. Le lysozyme se trouve dans les larmes, les crachats, la salive, le plasma et le sérum, les leucocytes, les protéines de poulet et les œufs de poisson. Le lysozyme se trouve en concentration la plus élevée dans les larmes et le cartilage. Le lysozyme n'a pas été détecté dans le liquide céphalo-rachidien, le cerveau, les selles ou la sueur. Le lysozyme dissout non seulement les microbes vivants mais aussi les microbes morts. En plus des saprophytes, il agit également sur certains microbes pathogènes (gonocoques, bacilles charbonneux), supprimant quelque peu leur croissance et provoquant une dissolution partielle. Le lysozyme n'a aucun effet sur les virus étudiés à cet égard. Le plus révélateur est le rôle du lysozyme dans l'immunité de la cornée, ainsi que de la cavité buccale, du pharynx et du nez. La cornée est un tissu extrêmement sensible aux infections, elle entre en contact direct avec un grand nombre de microbes de l'air, notamment ceux qui peuvent provoquer des suppurations (staphylocoques, pneumocoques). Cependant, ces maladies de la cornée sont relativement rares, ce qui peut s'expliquer par le caractère hautement bactéricide des larmes, qui lavent constamment la cornée, et par leur teneur en lysozyme. En raison de la teneur élevée en lysozyme de la salive, toutes sortes de plaies buccales guérissent inhabituellement rapidement. Si une surface aussi granuleuse, comme celle qui se produit par exemple lors d'une extraction dentaire, se trouvait dans une autre zone du corps, une infection serait inévitable. Cependant, malgré la présence d'un grand nombre de microbes dans le vortu, cela ne se produit pas. La nature bactéricide de la salive met en évidence l’instinct répandu chez tous les animaux de se lécher avec la langue. Ce léchage permet non seulement d'éliminer mécaniquement l'infection, mais également d'introduire un agent bactéricide dans la plaie. Dans le même temps, les animaux sont moins sensibles aux microbes introduits dans la plaie depuis la cavité buccale qu'aux infections étrangères. La fonction physiologique du lysozyme reste encore inexplorée.
Le rôle protecteur de la peau et des muqueuses est révélé par l'étude de la létalité comparée d'animaux sensibles infectés par la peau ou les muqueuses et contournant cette barrière. En plus du lysozyme, d’autres substances bactéricides ont été trouvées dans les tissus et les fluides.
Les propriétés bactéricides du lait ont été étudiées en détail par Wilson et Rosenblum (1952). Un facteur spécial appelé lacténine, bactéricide contre le streptocoque hémolytique, a été découvert dans le lait humain, de vache et de brebis. La lacténine est conservée lors de la pasteurisation, mais est détruite à partir de t0 800.
Toutes ces substances peu étudiées (lacténine, polypeptide, etc.) ne sont pas bactéricides au sens littéral du terme, tuant la cellule bactérienne en détruisant son protoplasme. Ils suppriment la prolifération des microbes, affectant apparemment leur métabolisme, comme les antibiotiques.
Dans certains cas, la présence dans les tissus de certains éléments formés lors du processus métabolique peut empêcher ou favoriser la prolifération de certains microbes. On sait, par exemple, que des concentrations insignifiantes de fer créent des conditions optimales pour la production de toxines par certaines souches de microbes diphtériques et que la teneur en fer des films diphtériques chez l'homme peut être nettement inférieure à cet optimal. Par conséquent, seules quelques souches peuvent provoquer des maladies graves chez l’homme en présence de concentrations de fer appropriées.
Inflammation et phagocytose.
Phagocytose – capture et absorption actives de cellules vivantes ou de petites particules par des organismes unicellulaires ou des cellules spéciales - les phagocytes. La phagocytose est l’une des réactions de défense de l’organisme, principalement contre l’inflammation. Découvert par I.I. Mechnikov en 1882.
Avec une virulence importante du microbe et avec une dose infectieuse suffisante, les barrières cutanées et muqueuses peuvent être totalement insuffisantes et le microbe pénètre dans la peau, les muqueuses ou la couche sous-cutanée ou sous-muqueuse. Dans un nombre important de cas, un processus inflammatoire se développe. L'étude du rôle de ce processus dans la protection de l'organisme contre les microbes est associée au nom de I.I. Mechnikov.
Mechnikov a étudié les fonctions des couches germinales, en particulier la couche germinale moyenne - le mésoderme chez les embryons d'animaux invertébrés ; en introduisant tout corps étranger (un capillaire de verre) dans le corps de l'éponge, il observa que celle-ci était entourée de cellules mobiles du mésoderme amiboïde capables d'avaler diverses particules inertes. Un processus similaire - l'afflux de leucocytes, leur entourage et l'absorption d'un corps étranger, provoquant un processus inflammatoire - a été observé chez d'autres espèces animales, avec ou sans système circulatoire. Ce processus d'absorption par les cellules des microbes et autres éléments corpusculaires I.I. Mechnikov l'appelait phagocytose. De nombreuses études réalisées avec divers microbes ont permis à Mechnikov de conclure à l'importance prédominante de la phagocytose dans les processus inflammatoires et à la fonction protectrice du processus inflammatoire lui-même. La phagocytose dans la réaction inflammatoire est en effet l'un des mécanismes de défense essentiels à tous les niveaux de l'échelle zoologique. Cependant, le mécanisme de protection de la réaction inflammatoire s’est avéré plus complexe qu’on pourrait le penser, et la phagocytose n’épuise pas toutes les possibilités de protection qu’apporte le processus inflammatoire. L'histamine et la sérotonine, libérées principalement par les mastocytes, jouent un rôle important dans le mécanisme de l'inflammation. Ils affectent la perméabilité des parois capillaires et de la substance principale du tissu conjonctif et renforcent l'activité phagocytaire de l'endothélium et du mésenchyme. Le facteur de perméabilité aux globulines et son inhibiteur, ainsi que de nombreuses autres substances telles que les enzymes qui évoluent à différentes étapes du processus inflammatoire, sont essentiels.
Les tissus enflammés sont également capables de fixer des protéines et des particules inertes. Une protéine étrangère introduite dans la zone d'inflammation de la peau ou dans la cavité abdominale est retenue plus longtemps que dans les tissus normaux, et la rétention dans la peau est plus longue. que dans la cavité abdominale. Des retards similaires à la source de l'inflammation ont été observés lors de l'introduction de peintures dans la cavité abdominale. Par conséquent, le processus inflammatoire, qu'il se produise dans un organisme immunisé ou non, empêche la dissémination des microbes. Il n'apparaît pas immédiatement après l'introduction d'un microbe, même dans les cas où le microbe, par exemple le staphylocoque, a la capacité de provoquer l'inflammation la plus grave. Si les microbes ont un pouvoir invasif élevé, certains d’entre eux pénètrent dans l’organisme avant que la réaction inflammatoire ne se produise et devienne si intense qu’elle peut empêcher la dissémination de l’agent pathogène. La fréquence d'apparition d'une réaction inflammatoire aiguë dépend de la nature du stimulus. Le stade du processus inflammatoire est également important. Les premiers stades de la réaction inflammatoire s'accompagnent d'une hyperémie active et d'un flux sanguin et lymphatique accéléré. Pendant cette période, les bactéries peuvent rapidement être emportées hors du site d'injection, ce qui peut contribuer au développement du processus infectieux. Cependant, cette étape est de très courte durée et les troubles vasculaires et l'afflux de leucocytes qui surviennent rapidement empêchent la propagation de l'infection. Ainsi, la réaction inflammatoire est un mécanisme de défense qui empêche la dissémination des microbes, mais elle n’intervient pas immédiatement après l’entrée des microbes dans l’organisme, mais après plusieurs heures. Au cours de la dernière étape du processus inflammatoire, lorsque d'énormes quantités de leucocytes s'accumulent dans la zone inflammatoire, une destruction intensive des microbes restants a lieu par phagocytose.
Le mécanisme de fixation et d'accumulation de microbes et de substances étrangères dans la zone d'inflammation est complexe. Le blocage lymphatique, qui se produit dans la zone inflammatoire en raison de la stase et de la coagulation lymphatique, est l'un des principaux facteurs empêchant la dissémination des microbes du foyer inflammatoire. Ce blocage forme une barrière mécanique constituée de plasma coagulé et représente un obstacle important au passage des microbes. Dans un processus inflammatoire aigu, il n'y a pas de ralentissement, mais une accélération du flux lymphatique à travers la zone d'inflammation, et des bactéries et autres particules étrangères se fixent dans cette zone sous l'action de divers facteurs physico-chimiques.
La phagocytose et les anticorps jouent un rôle important dans la fixation et la destruction des microbes dans le foyer inflammatoire.
Les leucocytes, qui s'accumulent en abondance dans la zone d'inflammation, forment une sorte de puits qui empêche la dissémination des organismes. Parallèlement à cela, les éléments cellulaires de la tige leucocytaire détruisent activement l'agent pathogène. Une augmentation de la pression capillaire et une augmentation de la perméabilité capillaire, qui se produisent lors de l'inflammation, provoquent une augmentation de la quantité de liquide pénétrant à travers l'endothélium des capillaires. La zone inflammatoire est enrichie de substances contenues dans le sang, dont des anticorps (normaux et immunitaires). Les anticorps, agissant sur les bactéries, les rendent plus accessibles aux facteurs de défense cellulaire et les maintiennent dans la zone inflammatoire. Il est possible que l'alexine, la bétalisine et d'autres facteurs de protection non spécifiques, concentrés dans la zone inflammatoire, jouent un rôle dans le mécanisme de protection complexe provoqué par la réponse inflammatoire.
Comme on le sait, la principale propriété des phagocytes est leur capacité à subir une digestion intracellulaire. Cependant, cette capacité ne s’exprime pas toujours et pas pour tous les microbes dans la mesure appropriée. Parfois, les microbes capturés par les phagocytes non seulement ne sont pas digérés par ceux-ci, mais s'y conservent et s'y multiplient (phagocytose incomplète). Dans ce cas, la phagocytose n'est pas une réaction protectrice de l'organisme, mais protège au contraire les microbes des propriétés bactéricides de l'organisme. Ce phénomène est cependant rare. Une autre caractéristique des phagocytes est leur chimiotaxie positive envers les microbes et leurs produits. La chimiotaxie positive permet de détruire les microbes pénétrant dans l'organisme par les leucocytes qui s'accumulent au site de leur pénétration. Cependant, de fortes doses de microbes ou de toxines peuvent provoquer une chimiotoxie négative, et la réaction phagocytaire ne peut alors pas être réalisée. Lors d'une réaction inflammatoire, il se produit une accumulation importante de leucocytes, qui traversent les parois des vaisseaux sanguins en raison de l'attraction chimiotoxique. Le pus qui s'accumule au cours des processus inflammatoires représente ces accumulations.
Mais même en l’absence d’inflammation, le rôle protecteur de la phagocytose peut être détecté de manière tout à fait démontrable. Lorsque des microbes sont introduits dans un animal immunisé, ces derniers sont immédiatement capturés par les phagocytes ; par exemple, en introduisant une culture de charbon chez une grenouille, on peut observer qu'au bout d'un certain temps tous les microbes sont phagocytés et que l'infection ne se développe pas. La même chose peut être observée lorsqu’une grande variété de microbes non pathogènes sont introduits dans un animal. Dans un organisme sensible, la phagocytose n'est pas observée du tout ou n'est observée que dans une faible mesure. Les phagocytes sont capables de capturer les microbes vivants. Si vous prélevez un exsudat d'une grenouille ayant reçu une culture de bacilles charbonneux, contenant des leucocytes ayant complètement capturé tous les bacilles, et que vous l'injectez à un cobaye, celui-ci mourra du charbon, puisque les leucocytes de la grenouille, ayant se retrouvent dans un environnement inadapté dans le corps du cobaye, meurent et libèrent ainsi ceux qui y sont emprisonnés. Ce sont des microbes assez virulents. La preuve de l’importance incontestable de la phagocytose en tant que mécanisme de protection de l’organisme est également le fait que la suppression du phagocyte ou la création d’obstacles à son développement réduisent la résistance de l’organisme. Si les spores du tétanos sont soigneusement éliminées de la toxine et introduites dans le corps de l'animal, elles sont alors rapidement phagocytées et la maladie tétanique ne se produira pas. Cependant, si ces spores sont introduites dans un coton-tige, alors que les leucocytes ne peuvent pas les absorber ou le font trop tard, les spores ont le temps de germer et la maladie et la mort surviennent. Si une culture microbienne est introduite avec de l'acide lactique, qui a un effet chimique toxique négatif sur les leucocytes, la mort surviendra à partir d'une dose de culture facilement tolérée par les animaux sans acide. En revanche, une augmentation du nombre de leucocytes, notamment au niveau du site de l'infection, augmente sans aucun doute la résistance de l'organisme. Elle peut également être causée par des agents non spécifiques. Il ne fait aucun doute que la leucocytose est l'un des facteurs de l'immunité non spécifique, qui est reproduite par ce qu'on appelle la thérapie protéique.
La liaison (adsorption) des toxines par les leucocytes a été décrite à plusieurs reprises par différents auteurs en relation avec les toxines diphtérique et tétanique, bien que les résultats obtenus soient assez contradictoires.
La réaction de phagocytose n'a pas de fonction protectrice dans toutes les maladies infectieuses : par exemple, dans la méningite provoquée par le bacille de la grippe, ce dernier est absorbé mais non détruit par les phagocytes, qui le protègent de l'action des anticorps. Mais dans la grande majorité des infections bactériennes, la phagocytose a, à un degré ou à un autre, des fonctions protectrices. La phagocytose a une signification différente dans les infections virales : la réaction phagocytaire n'est pas équivalente dans tous les processus infectieux. Ceci est tout à fait conforme aux vues de I.I. Mechnikov, qui, en étudiant les réactions phagocytaires chez divers animaux et avec divers microbes, a établi diverses formes de cette réaction au cours de son développement évolutif. Les staphylocoques sont capturés et tués par les leucocytes, les gonocoques sont phagocytés par eux mais restent vivants à l'intérieur des leucocytes et enfin, certains virus ne sont pas du tout phagocytés par les leucocytes. Il est possible que ces trois exemples représentent trois étapes différentes dans le développement évolutif des leucocytes. réaction phagocytaire.
RÉGULATION DE L'IMMUNITÉ.
L'intensité de la réponse immunitaire est largement déterminée par l'état des systèmes nerveux et endocrinien. Il a été établi que l'irritation de diverses structures sous-corticales (thalamus, hypothalamus, tubercule gris) peut s'accompagner à la fois d'une augmentation et d'une inhibition de la réponse immunitaire à l'introduction d'antigènes. Il a été démontré que la stimulation de la partie sympathique du système nerveux autonome (végétatif), ainsi que l'administration d'adrénaline, améliorent la phagocytose et l'intensité de la réponse immunitaire. Une augmentation du tonus de la division parasympathique du système nerveux autonome conduit à des réactions opposées.
Le stress, ainsi que la dépression, suppriment le système immunitaire, ce qui s'accompagne non seulement d'une susceptibilité accrue à diverses maladies, mais crée également des conditions favorables au développement de néoplasmes malins.
Ces dernières années, il a été établi que l'hypophyse et la glande pinéale, à l'aide de biorégulateurs peptidiques spéciaux appelés « cytomédines », contrôlent l'activité du thymus. Le lobe antérieur de l'hypophyse est un régulateur principalement cellulaire, et le lobe postérieur de l'immunité humorale.
SYSTÈME IMMUNITAIRE DE RÉGULATION.
Récemment, il a été suggéré qu'il n'existait pas deux systèmes de régulation (nerveux et humoral), mais trois (nerveux, humoral et immunitaire). Les cellules immunocompétentes sont capables d'interférer avec la morphogenèse et de réguler le cours des fonctions physiologiques. Un rôle particulièrement important dans la régulation des fonctions physiologiques appartient aux interleukines, qui constituent « une famille de molécules pour toutes les occasions », car elles interfèrent complètement avec les processus physiologiques se déroulant dans l'organisme.
Le système immunitaire est un régulateur de l'homéostasie. Cette fonction est réalisée grâce à la production d'auto-anticorps qui se lient aux enzymes actives, aux facteurs de coagulation sanguine et aux hormones en excès.
La réaction immunologique, d'une part, fait partie intégrante de la réaction humorale, puisque la plupart des processus physiologiques et biochimiques sont réalisés avec la participation directe d'intermédiaires humoraux. Cependant, la réaction immunologique est souvent ciblée et s’apparente donc à une réaction nerveuse. Les lymphocytes et les monocytes, ainsi que d'autres cellules participant à la réponse immunitaire, libèrent des médiateurs humoraux directement vers l'organe cible. D'où la proposition de qualifier la régulation immunologique de cellulaire-humorale.
La prise en compte des fonctions régulatrices du système immunitaire permet aux médecins de diverses spécialités d'adopter une nouvelle approche pour résoudre de nombreux problèmes de médecine clinique.
Fonction barrière du tissu lymphatique. Microbe qui a pénétré la peau et les barrières muqueuses. Dans la grande majorité des cas, il pénètre dans les ganglions lymphatiques. Le streptocoque hémolytique, introduit dans le vaisseau lymphatique menant au ganglion lymphatique, est retenu en quantité importante dans ce ganglion et est quasiment indétectable dans le vaisseau sortant. Des résultats similaires ont été obtenus lors d'expériences avec de nombreux autres microbes en les introduisant sous la peau, dans le les poumons et dans les intestins. Mais lorsque des bactéries étaient introduites dans la cavité péritonéale, on observait leur apparition très rapide dans le sang. Les observations de propagation des bactéries dans l'organisme introduites sous la peau montrent que les ganglions lymphatiques constituent une barrière qui empêche la pénétration des bactéries dans l'organisme. La fonction barrière des ganglions lymphatiques augmente avec la vaccination. Cette question a été étudiée en détail par V.M. Berman (1948) et d'autres chercheurs. Ils ont découvert que lorsque des animaux de laboratoire étaient infectés par la fièvre typhoïde, la dysenterie, la tuberculose, la brucellose et le choléra, les ganglions lymphatiques , vaisseaux endothéliaux et cellules réticulo -les systèmes endothéliaux ont une capacité prononcée dans le corps immunitaire à empêcher la pénétration de bactéries dans le corps. La capacité du tissu lymphatique à empêcher la pénétration de microbes dans le corps est appelée fonction de fixation de barrière. Certaines bactéries retenues dans les ganglions lymphatiques s'y multiplient. Ainsi, les observations de H.H. Planels (1950) ont montré que les microbes typhoïdes se multiplient vigoureusement dans les ganglions lymphatiques, pénétrant dans les lymphocytes et formant des colonies dans leurs noyaux. La fonction barrière des ganglions lymphatiques est dans une certaine mesure associée au processus inflammatoire provoqué par des bactéries envahissantes.
Réactivité immunologique – la capacité de l’organisme à répondre à la prolifération des antigènes change sous l’influence de divers facteurs, ainsi qu’avec l’âge. Les animaux nouveau-nés ont une réactivité immunologique fortement réduite, ce qui explique leur susceptibilité accrue à de nombreuses infections. Les changements dans la réactivité du corps qui se produisent avec l'âge en relation avec la capacité à former des anticorps ont été notés par I.I. Mechnikov.
En 1897, il observa que les crocodiles adultes produisaient de l'antitoxine tétanique à des concentrations nettement plus élevées que les juvéniles. Par la suite, de nombreux auteurs ont observé l'absence d'anticorps ou une forte diminution de leur formation chez les animaux nouveau-nés et une augmentation de cette capacité chez les animaux adultes. Par exemple, chez le lapin, avec l'âge, on observe une augmentation de la production d'anticorps contre de nombreux antigènes (anti-sérum de cheval, érythrocytes de mouton, vaccin contre la typhoïde).
Une capacité d'immunisation plus prononcée chez les animaux adultes a également été démontrée dans des expériences sur des rats porteurs de trypanosomes, sur des souris atteintes d'encéphalomyélite et de virus de la rage, et dans d'autres cas similaires. Dans le même temps, il a été noté que la capacité à produire des anticorps chez les lapins âgés est moins prononcée que chez les lapins d'âge moyen. La capacité de phagocytose est également fortement réduite chez les nouveau-nés. Apparemment, dans tous ces cas, il existe une diminution primaire de la réactivité associée à la biochimie des cellules nouveau-nées. Une diminution de réactivité encore plus prononcée se produit au cours de la vie embryonnaire. Dans l'embryon de poulet en développement, les anticorps ne se forment pas du tout ou se forment à un titre insignifiant. Parallèlement, de nombreux agents infectieux auxquels les animaux adultes ne sont pas sensibles se multiplient dans les embryons. Cette reproduction est si intense que les embryons de poulet sont largement utilisés pour obtenir des cultures virales. De nombreuses bactéries se reproduisent également dans les embryons de poulet. Récemment, du matériel expérimental s'est accumulé, indiquant la présence d'une réactivité immunologique particulière dans la vie embryonnaire.
Pathologie de l'immunité.
Pendant longtemps, il a été considéré comme établi que l’organisme ne réagissait pas en formant des anticorps contre ses propres antigènes. Ehrlich considérait cela comme une manifestation d’une sorte de « peur de l’auto-empoisonnement ».
Cependant, peu à peu, des preuves se sont accumulées indiquant que, dans certains cas, l'organisme peut produire des anticorps contre ses propres antigènes. Un phénomène similaire se produit si les propres antigènes de l'organisme sont dénaturés par un processus pathologique et pénètrent sous une forme altérée dans les tissus qui produisent des anticorps, ou si ces tissus reçoivent des antigènes qui, dans des conditions naturelles, ne pénètrent jamais dans le sang et ont une spécificité d'espèce réduite (par exemple). exemple, les protéines du cristallin). De tels auto-antigènes provoquent un processus d'auto-immunisation dans leur propre corps, conduisant à un certain nombre de conditions pathologiques, parfois très graves, en raison de la réaction entre les auto-anticorps qui en résultent.
Les processus immunologiques visent généralement à restaurer la relative constance de l'environnement interne de l'organisme, associée à leur fonction protectrice. Dans les cas présentés, ces processus conduisent à une violation de la constance de l'environnement interne, qui s'exprime par un certain nombre de phénomènes cliniques de nature pathologique. Par conséquent, tous ces troubles provoqués par des processus immunologiques peuvent être regroupés sous le concept général de pathologie immunitaire. Actuellement, un certain nombre de maladies ont été étudiées, dont l'apparition est associée ou associée au processus d'auto-immunisation. Ceux-ci comprennent : l'anémie hémolytique acquise, l'ictère physiologique, la cardite rhumatismale et d'autres maladies. Les anticorps qui apparaissent dans certaines de ces maladies ont été relativement bien étudiés.
sida
L'un des problèmes les plus importants et les plus urgents de l'humanité moderne sont les maladies de civilisation (cancer, sida, syphilis, toxicomanie et alcoolisme, etc.). Les médecins ont lutté longuement et durement contre bon nombre d’entre eux, mais n’ont malheureusement toujours pas trouvé d’antidotes. L'une de ces maladies est le SIDA : syndrome d'immunodéficience acquise.
C’est ce qu’on appelle la peste de notre siècle. Elle est causée par le virus de l'immunodéficience humaine (VIH), qui attaque le système de défense de l'organisme.
L'épidémie de sida dure depuis environ 20 ans : on pense que les premiers cas massifs d'infection par le VIH se sont produits à la fin des années 1970. Bien que le VIH ait depuis été mieux compris que n’importe quel virus dans le monde, des millions de personnes continuent de mourir du SIDA et des millions d’autres reçoivent un diagnostic d’infection par le VIH. Le sida est l’une des cinq principales maladies mortelles qui font le plus grand nombre de morts sur notre planète. L'épidémie continue de croître, couvrant de plus en plus de régions. Des études sociologiques ont montré que plus de 20 millions de personnes sont mortes du virus (en 20 ans de recherche), 40 millions vivent avec ce terrible diagnostic.
Ces dernières années, non seulement les connaissances sur le VIH et le sida ont changé, mais aussi l’attitude de la société face à ce problème. De l’ignorance et de la peur aveugle de cette maladie, l’humanité est parvenue à une victoire partielle de la science sur le virus et du bon sens sur la dysstérie et la speedophobie.
Origine du virus de l'immunodéficience
Le corps humain possède une immunité - une série de réactions protectrices dirigées contre les agents infectieux. Les principales cellules du système immunitaire sont les microphages (« phage » en grec – manger) et les lymphocytes. Le système immunitaire fonctionne ainsi : il reconnaît et élimine tout ce qui est étranger au corps - microbes, virus, champignons et même ses propres cellules et tissus, s'ils deviennent étrangers sous l'influence de facteurs environnementaux (« immunités » - libres de tout). Le système immunitaire est très efficace et ingénieux. Cependant, cela ne peut pas aider l’organisme dans tous les cas. L’un des virus auxquels le système immunitaire ne peut pas résister est le virus de l’immunodéficience humaine.
Avant de comprendre comment fonctionne le virus VIH, vous devez parler un peu du sang. Le sang est un tissu conjonctif liquide constitué de plasma et d'éléments formés individuels : globules rouges - érythrocytes, globules blancs - leucocytes et plaquettes sanguines - plaquettes. Dans l'organisme, le sang remplit diverses fonctions : respiratoire, nutritionnelle, excrétrice, thermorégulatrice, protectrice, humorale. Ce que l'on appelle l'immunité cellulaire est assurée par les lymphocytes T. Leur variété - les T-killers (« tueurs ») sont capables de détruire les cellules contre lesquelles des anticorps ont été produits ou de tuer des cellules étrangères. Des réactions immunitaires complexes et diverses sont régulées par deux autres types : les lymphocytes T : les T-helpers (« assistants »), également appelés T4, et les T-suppresseurs (« oppresseurs »), autrement appelés T8. Les premiers stimulent les réactions immunitaires cellulaires, les seconds les inhibent.
La cause du SIDA est donc l’infection par le VIH. Bien que certains aspects de l’infection par le VIH ne soient pas encore entièrement compris, comme la manière exacte dont le virus détruit le système immunitaire et la raison pour laquelle certaines personnes séropositives restent en parfaite santé pendant de longues périodes, le VIH est l’un des virus les plus étudiés de l’histoire de l’humanité. Le virus de l’immunodéficience appartient aux lentivirus (« virus lents »), un sous-groupe de rétrovirus. Ces virus sont dits lents parce que leur période d’incubation se mesure en mois et en années et parce que la maladie a une évolution longue et chronique.
Une fois dans l'organisme, le VIH attaque certaines cellules sanguines : les lymphocytes T - « assistants ». À la surface de ces lymphocytes se trouvent des molécules CD-4, c'est pourquoi on les appelle aussi lymphocytes T-4 et lymphocytes CD-4 (ou Cellules CD-4).
La structure du virus est primitive : une coque constituée d'une double couche de molécules de graisse, des « champignons » glycoprotéiques qui en poussent, à l'intérieur se trouvent deux chaînes d'ARN contenant le programme génétique du virus, et des protéines - transcriptase inverse, intégrase et la protéase. Hormis ce maigre bagage, le virus n’a besoin de rien : il utilise la cellule hôte pour se reproduire.
L’information génétique de la plupart des cellules et virus naturels est codée sous forme d’ADN. Dans le VIH, il est codé dans l’ARN. Le virus doit traduire ses informations génétiques dans un langage compréhensible par la cellule hôte, c'est-à-dire traduire son ARN en ADN. Pour ce faire, le virus utilise une enzyme appelée transcriptase inverse, qui convertit l'ARN en ADN. Après une telle transformation, la cellule hôte accepte l’ADN du virus « comme s’il s’agissait du sien ». Ce processus se produit généralement dans les 12 heures suivant l'infection.
Le virus est décrit comme ressemblant à une mine anti-sous-marine. Les « champignons » à sa surface sont constitués de molécules glycoprotéiques. Le « chapeau » est constitué de trois à quatre molécules de GP120 et la « jambe » est constituée de 3 à 4 molécules de GP41.
Nombre de personnes infectées par le VIH dans le monde :
AUSTRALIE 12 000 AMÉRIQUE DU NORD 920 000 AMÉRIQUE DU SUD 1,3 million EURASIE 7,4 millions AFRIQUE 23,5 millions TOTAL 33,6 millions
Comment peut-on être infecté par le SIDA ??
1. Grâce à une aiguille d'injection intraveineuse. Par exemple, lorsque la même aiguille est utilisée par plusieurs personnes qui s'injectent des drogues. Chaque fois après une injection intraveineuse, il y a un peu de sang dans l'aiguille - si peu qu'il n'est pas toujours visible, mais suffisamment transmettre la maladie à la prochaine personne qui s'injecte l'aiguille dans une veine.
2. Pendant une transfusion sanguine. Cela se produit dans les rares cas où le sang de personnes infectées par le VIH, qui n'a pas été correctement testé, est utilisé à cette fin. Il existe désormais des tests assez fiables permettant de déterminer la présence du virus dans le sang.
3. De la mère à l'enfant : Une femme enceinte infectée peut infecter son enfant à naître car ils partagent le même système circulatoire. Cependant, cela se produit désormais extrêmement rarement, car toutes les femmes enceintes doivent subir un test de dépistage du VIH.
sida tu ne peux pas être infecté à travers:
toucher et serrer la main ;
embrasser (si les deux n'ont pas de blessures ouvertes dans la bouche) ;
Piqure de moustique; en toussant et en éternuant ;
siège de toilette, vaisselle et autres choses.
Lorsqu'elles sont infectées par le VIH, la plupart des gens ne ressentent aucune sensation. Parfois, quelques semaines après l'infection, un état pseudo-grippal apparaît (fièvre, éruptions cutanées, gonflement des ganglions lymphatiques, diarrhée).
Quelques symptômes de l'infection par le VIH : toux sèche persistante ; fièvre prolongée, plus de trois mois, de cause inconnue ; transpirer la nuit; perte de poids soudaine ; maux de tête fréquents, faiblesse, diminution de la mémoire et des performances ; inflammation de la muqueuse buccale, plaque blanchâtre, ulcères ; diminution inexpliquée de la vision et cécité.
Cependant, si une personne présente l’un des symptômes décrits ici, cela ne signifie pas qu’elle est atteinte du SIDA. Ces symptômes peuvent être causés par d’autres maladies non liées à l’infection par le VIH. Vous devez donc toujours vous faire tester et découvrir la cause de la maladie. Dans tous les cas, une décision raisonnable serait de consulter un médecin.
À ce jour, le SIDA reste l’une des maladies les plus dangereuses de l’humanité. Qu’est-ce qui fait de cette maladie l’une des plus insidieuses ? Le fait que les médecins et les scientifiques n’ont pas encore trouvé d’antidote. Toutes leurs tentatives ont jusqu’à présent été vaines. Mais grâce au travail minutieux des médecins et des scientifiques du monde entier, des médicaments sont apparus qui aident à prolonger la vie d'une personne infectée.
Aujourd'hui, dans presque toutes les librairies, vous pouvez acheter de la littérature qui explique dans un langage simple, compréhensible non seulement pour un spécialiste de l'étude de cette maladie, mais aussi pour toute personne, cette terrible maladie, son développement et ses conséquences. Mais la plupart des gens soit n’écoutent pas les conseils médicaux, soit croient que cela ne leur arrivera jamais. C’est peut-être précisément cette attitude frivole à l’égard de la santé et le non-respect des précautions de base qui ont conduit au fait que le SIDA gagne en force de manière alarmante et reste l’une des maladies les plus courantes que l’humanité ait jamais connues.
Il me semble que le SIDA peut être vaincu, mais pour y parvenir, nous devons vaincre une autre maladie plus ancienne. Notre ignorance.
Littérature
1. Bakoulev A.N., Brusilovsky L.Ya., Timakov V.D., Shabanov A.N.
Grande Encyclopédie Médicale M., 1959.
2. Khlyabich G., Zhdanov V. SIDA : connaître et combattre. "Médical
3. Kudryavtseva E., Le SIDA de 1981 à... « Science et Vie » n° 10, 1987.
4.V.M. Pokrovsky V.M., Korotko G.F., Physiologie humaine M,
5. Données du site Web www.mednovosti.ru
La protection de l'organisme contre les infections est assurée non seulement par la phagocytose, mais également par des facteurs humoraux, c'est-à-dire par la formation dans les cellules de substances qui neutralisent les microbes et leurs produits métaboliques. Ainsi, dans certaines maladies causées par des microbes (maladies infectieuses), le corps produit et accumule des substances (antitoxines) qui neutralisent (probablement par liaison chimique) les poisons bactériens - les toxines. Après des injections répétées de toxines dans le sang des animaux, les antitoxines correspondantes s'y accumulent. Le sérum sanguin de ces animaux est utilisé à des fins médicinales.
Dans de nombreuses maladies infectieuses (par exemple la rougeole, la variole, le typhus, etc.), des substances appelées anticorps ou corps immunitaires se forment dans l'organisme, empêchant le développement de micro-organismes. En conséquence, certaines maladies réapparaissent rarement chez la même personne. Le sérum sanguin d'une personne rétablie a un effet déprimant sur les agents pathogènes de cette maladie. L'état d'immunité contre la maladie dû à la présence dans le sang et les tissus de substances qui empêchent le développement d'une infection et à des modifications dans la capacité des cellules du corps à répondre aux agents pathogènes est appelé immunité. Les anticorps sont produits par les leucocytes et les cellules du système réticuloendothélial.
La formation de corps immunitaires ne peut pas être causée uniquement par des microbes. Lorsqu’une protéine étrangère est introduite par voie parentérale (c’est-à-dire en contournant le tube digestif) dans l’organisme, des anticorps apparaissent également dans le sang. Lorsque le sérum d'un animal immunisé agit sur la protéine étrangère contre laquelle il est immunisé, celle-ci coagule et tombe sous forme de flocons. Ce phénomène est appelé précipitation et les substances qui le provoquent sont appelées précipitines. Les corps immunitaires comprennent également les hémolysines, les agglutinines, etc.
Dans les cas où des corps immunitaires sont présents dans le corps dès la naissance, on parle d'immunité innée ou héréditaire. L’accumulation de corps immunitaires au cours de la vie d’un individu est appelée immunité acquise. L'immunité héréditaire explique l'immunité de l'homme et de certaines espèces animales face à certaines maladies. Ainsi, une personne ne contracte pas la peste bovine. Les influences extérieures peuvent perturber l’immunité innée. Les poulets, qui sont normalement immunisés contre le charbon, en tombent malades s'ils sont exposés à la réfrigération. Les rayonnements ionisants réduisent également la résistance du corps aux infections.
L’immunité innée est largement déterminée par la capacité des leucocytes à phagocyter. Après avoir injecté à un lapin des spores du charbon, celles-ci sont capturées et détruites par les globules blancs qui les digèrent. Dans le sérum sanguin de lapin, les spores de la bactérie du charbon se développent bien.
Anaphylaxie. Lorsque des substances étrangères de nature protéique qui lui sont étrangères rentrent dans le corps, une condition particulière appelée anaphylaxie se produit.
Par exemple, si pour la première fois une petite quantité de sérum étranger (0,02 ml) est injectée à un cobaye sous la peau, dans le sang ou par voie intrapéritonéale, aucun effet nocif ne sera constaté. Mais si après 15-20 jours l'administration du même sérum est répétée, une réaction violente se produit et un état grave survient - choc anaphylactique, accompagné de convulsions, de problèmes respiratoires et cardiaques et se terminant par la mort quelques minutes après l'administration du sérum. . Cela se produit parce que la première introduction d'une protéine étrangère provoque un état de sensibilité accrue de l'animal à cette protéine (injection sensibilisante). L'administration répétée de la même substance protéique agit sur un animal aussi sensibilisé que l'introduction d'un poison puissant (injection permissive).
Si l’animal survit à l’injection permissive, alors il est désensibilisé, c’est-à-dire libéré de l’état d’hypersensibilité créé par l’injection sensibilisante. Les mécanismes d’apparition de ces conditions sont complexes et mal compris.