Thyroïde produit les hormones thyroïdiennes thyroxine et triiodothyronine, ainsi que la thyrocalcitonine (calcitonine).
Thyroxine Et triiodothyronine sont de puissants stimulateurs des processus oxydatifs dans les cellules, et la triiodothyronine est 5 à 10 fois plus active que la thyroxine. Ces hormones améliorent le métabolisme, la synthèse des protéines, les échanges gazeux, le métabolisme des glucides et des graisses. Les hormones thyroïdiennes ont un effet significatif sur le développement, la croissance et la différenciation des cellules et des tissus. Ils accélèrent le développement le tissu osseux. Les hormones thyroïdiennes ont une influence particulièrement grande sur l'histogenèse du tissu nerveux. Lorsque la glande thyroïde est insuffisante, la différenciation des cellules et des tissus du cerveau est inhibée et le développement mental d’une personne est perturbé.
Les hormones thyroïdiennes avoir un effet stimulant sur les processus de régénération des tissus. La composition de la thyroxine et de la triiodothyronine comprend l'iode comme ingrédient obligatoire, donc l'apport d'iode avec de l'eau potable et de la nourriture dans le corps est nécessaire au fonctionnement normal de la glande thyroïde. La troisième hormone thyroïdienne, la thyrocalcitonine, qui ne contient pas d'iode, participe à la régulation du métabolisme du calcium et du phosphore.
Développement de la glande thyroïde.
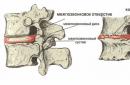
Rudiment thyroïdien apparaît dès la 4ème semaine d'embryogenèse sous la forme d'une saillie de la paroi ventrale de l'intestin pharyngé entre la 1ère et la 2ème paire de poches branchiales. Cette saillie se transforme en cordon épithélial avec un épaississement à son extrémité. La glande thyroïde est initialement formée comme une glande exocrine. Plus tard, le canal reliant la glande au pharynx est réduit et de ce canal il ne reste que le foramen caecum. Le cordon épithélial bifurque à son extrémité. Au cours du 3ème mois, des constrictions se forment le long des cordons épithéliaux. Des jeux apparaissent dans les segments distincts de ces cordons. À mesure que les constrictions s’approfondissent, les brins épithéliaux se brisent en follicules séparés et en îlots cellulaires.
A la fin du 3ème mois l'épithélium follicules différencie. Ses cellules - les endocrinocytes folliculaires (thyrocytes) - commencent à produire des hormones qui s'accumulent dans la cavité du follicule. La formation de nouveaux follicules et leur développement se produisent de manière hétérochrone. Au moment de la naissance, on note la présence de follicules avec colloïde (« structure de type colloïde ») et sans colloïde avec desquamation de l'épithélium (« structure de type desquamatif »). Entre les follicules se trouvent des îlots de cellules interfolliculaires. Au cours du développement de la glande, parallèlement à la différenciation de l'épithélium, le mésenchyme se développe et se transforme en tissu conjonctif. Le stroma de la glande se forme, contenant un réseau dense de capillaires. Les fibres nerveuses pénètrent dans le stroma.
Dans le rudiment de la glande les dérivés de la 5ème paire de poches branchiales se développent également dans les cellules des corps dits ultimobranchiaux. Ce sont des cellules C qui produisent de la calcitonine. Ce sont des cellules de nature neuroectodermique et elles pénètrent dans la glande thyroïde par les primordiums ultimobranchiaux.
Ainsi, dans la formation de structures et de fonctionnalités unités thyroïdiennes les différences cellulaires suivantes sont impliquées : ce sont les cellules principales de l'épithélium folliculaire - les endocrinocytes folliculaires qui produisent la thyroxine et la triiodothyronine ; calcitoninocytes, ou cellules C, produisant de la calcitonine et d'autres peptides (somatostatine, thyréolibérine, sérotonine, etc.).
La structure de la glande thyroïde.
Glande, constitué de deux lobes, est recouvert à l'extérieur d'une capsule de tissu conjonctif, à partir de laquelle s'étendent des septa, divisant le parenchyme en lobules. L'unité structurelle et fonctionnelle de la glande thyroïde est le follicule. Le diamètre moyen des follicules est d'environ 50 microns. Leur forme est majoritairement ronde. Les follicules sont des vésicules fermées. Leur paroi est formée d'un épithélium monocouche constitué d'endocrinocytes folliculaires (thyrocytes). Parmi ces cellules, sous forme de petits amas, se trouvent les cellules C. Ils peuvent se trouver à proximité des follicules et entre les follicules.
Cavité folliculaire rempli du produit de sécrétion des thyrocytes - un colloïde contenant des protéines - des thyroglobulines. À l’extérieur, les follicules sont entrelacés de réseaux de capillaires sanguins et lymphatiques. Entre les follicules adjacents se trouvent des îlots interfolliculaires constitués d'endocrinocytes peu différenciés.
Endocrinocytes folliculaires Ils ont une forme cubique et un noyau arrondi. Il y a des microvillosités sur leur surface apicale. Les organites assurant la synthèse des protéines sont bien développés dans le cytoplasme. Il existe de nombreux ribosomes libres qui forment des polysomes. Les endocrinocytes adjacents dans la paroi folliculaire sont reliés par des jonctions serrées, des desmosomes et des interdigitations.
Fonctionnalité histophysiologie de la glande thyroïde est le mouvement des produits de sécrétion dans des directions différentes : d'abord dans la cavité folliculaire, puis dans la direction opposée - dans le sang. Cela se produit grâce à travail actif endocrinocytes folliculaires. Le cycle de sécrétion de ces cellules comprend les phases suivantes : absorption des substances de départ, synthèse de la sécrétion, sa libération dans la cavité folliculaire sous forme de colloïde, iodation du colloïde, endocytose du colloïde iodé et sa modification et excrétion de l'hormone à travers la partie basale de la cellule dans les tissus et les vaisseaux sanguins environnants. capillaires lymphatiques. La production d'hormones thyroïdiennes commence par la synthèse de thyroglobuline dans la partie basale des endocrinocytes.
Contenant thyroglobuline les produits de synthèse issus du réticulum endoplasmique pénètrent dans le complexe de Golgi puis sont excrétés dans la cavité folliculaire sous forme de granules sécrétoires par exocytose. Un premier atome d'iode est ajouté à la thyroglobuline non iodée, puis un second, ce qui entraîne la formation de mono- et diiodothyronines. La complexation ultérieure produit de la tétraiodothyronine ou thyroxine. Lorsqu'un atome d'iode est retiré de la thyroxine, de la triiodothyronine se forme.
Dans des conditions normales, les processus éducation le colloïde et sa résorption sont équilibrés. Cet équilibre est cependant perturbé par l’hypo- et l’hyperfonctionnement de la glande thyroïde. En cas d'hypofonction, la libération de l'hormone est retardée. Dans ce cas, les follicules sont généralement gros, il y a beaucoup de colloïde dans la cavité du follicule, il est épais, n'a pas de vacuoles de résorption, l'épithélium est représenté par des endocrinocytes plats. En cas d'hyperfonctionnement, au contraire, la libération de l'hormone colloïdale dans le sang augmente. Le colloïde se liquéfie, sa quantité est faible, l'épithélium de la paroi folliculaire devient hautement prismatique.
Parafolliculaire endocrinocytes(Les cellules C ou calcitoninocytes) produisent l’hormone protéique calcitonine. Il abaisse le taux de calcium dans le sang et est un antagoniste de la parathyrine. La calcitonine agit sur les ostéoclastes du tissu osseux, réduisant ainsi leur activité de résorption. Les cellules C sont plus légères et plus grosses que les endocrinocytes folliculaires et leur proportion est de 0,1 %. Ils dorment généralement seuls ou en petits groupes. Le cytoplasme des endocrinocytes parafolliculaires contient de nombreux granules sécrétoires argyrophiles ou osmiophiles contenant de la calcitonine et d'autres peptides.
Stroma glandes se compose de tissu conjonctif fibreux lâche, dans lequel se trouvent souvent des mastocytes, des macrophages et des lymphocytes. Les fibroblastes de la glande thyroïde possèdent un certain nombre de propriétés uniques, qui est déterminé par les caractéristiques du système récepteur-transducteur des cellules. Ils peuvent notamment participer au développement de l’inflammation aux côtés des cellules immunocompétentes. Les capillaires fenestrés sont bien développés. Les fibres nerveuses contiennent des peptides caractéristiques des cellules C.
Réactivité. La régénération physiologique de la glande thyroïde se produit par le renouvellement des cellules épithéliales folliculaires dû à leur mitose. La source du développement de nouveaux follicules peut être des îlots cellulaires interfolliculaires. L'intoxication, les traumatismes, les processus auto-immuns, les facteurs héréditaires, etc. peuvent conduire à une thyréotoxicose ou à une hypothyroïdie. Il convient de garder à l'esprit que pour fonctionnement normal La glande thyroïde nécessite un apport suffisant en iode. La glande thyroïde a une grande capacité à se régénérer après une blessure. Un exemple de maladie thyroïdienne auto-immune est la maladie de Hashimoto. Cela est dû au fait que la thyroglobuline pénètre dans le stroma de la glande thyroïde et, en tant qu'antigène, provoque une réponse immunitaire dans le corps.
(glandula thyroïde) - une glande endocrine, qui fait partie du système endocrinien, maintient l'homéostasie du corps grâce à la production d'hormones spéciales. La glande thyroïde est un organe constitué de deux lobes adjacents à la trachée sur des côtés différents, et d'un isthme situé entre eux sur la face antérieure de la trachée. Dans certains cas, il peut y avoir un lobe pyramidal supplémentaire provenant de l’isthme ou du lobe gauche.
La glande thyroïde comprend également des capsules de tissu conjonctif : externes et internes. À l'aide de la capsule externe, un appareil ligamentaire se forme qui fixe la glande au larynx et à la trachée. Limite supérieure Les glandes (lobes latéraux) sont le cartilage thyroïde, celle du bas est constituée des 5 à 6 anneaux de la trachée. L'isthme est situé au niveau du cartilage trachéal I-III ou II-IV.
La taille de la glande thyroïde est normale
Le poids approximatif de la glande thyroïde est de 20 à 60 g. De plus, la taille de ses lobes peut varier dans la plage des paramètres suivants : 5-8 x 2-4 x 1-3 cm.
Le poids de la glande thyroïde augmente légèrement pendant la puberté, mais diminue avec la vieillesse. Chez les femmes, la glande thyroïde est plus grande que chez les hommes. Pendant la grossesse, une hypertrophie de la glande est observée. Ce phénomène disparaît progressivement de lui-même après l'accouchement.
Fonctions thyroïdiennes
La glande thyroïde est l’un des organes les plus importants responsables de l’approvisionnement en sang. Il a développé des systèmes artériels et veineux. Le sang pénètre dans la glande par deux artères thyroïdiennes supérieures (branches de l'artère carotide externe) et deux artères thyroïdiennes inférieures, qui forment des anastomoses entre elles. Les systèmes veineux et lymphatique assurent l'écoulement du sang et de la lymphe de la glande thyroïde, contenant des hormones thyroïdiennes, de la thyroglobuline et, dans des conditions pathologiques, des anticorps antithyroïdiens, des immunoglobulines stimulant la thyroïde et bloquant la thyroïde.
La glande thyroïde est innervée par des branches nerf vague(parasympathique) et branches des ganglions cervicaux (sympathiques).
Les follicules sont considérés comme l’unité fonctionnelle et structurelle clé de la glande thyroïde. Ce sont des bulles, dans la plupart des cas de forme ronde et d'un diamètre de 25 à 500 microns. Les follicules sont séparés les uns des autres par de fines couches de tissu conjonctif lâche avec un grand nombre de capillaires sanguins et lymphatiques.
Leur lumière est remplie de colloïde - une masse sans structure contenant de la thyroglobuline, qui est synthétisée par les cellules folliculaires, ou cellules A, formant la paroi du follicule. Ces cellules épithéliales ont une forme cubique ou cylindrique (avec une activité fonctionnelle accrue). Ils s'aplatissent si la fonction thyroïdienne diminue.
Outre les follicules, la glande thyroïde contient des îlots interfolliculaires de cellules épithéliales (cellules B, cellules Askanasi), qui sont également la principale source de formation de nouveaux follicules. Les cellules Askanasi sont plus grandes que les cellules A, ont un cytoplasme zosinophile et un noyau arrondi situé au centre : le cytoplasme contient des amines biogènes, ainsi que de la sérotonine. En plus des cellules A et B, la glande thyroïde contient des cellules parafolliculaires (cellules C). Elles sont situées sur la surface externe des follicules, sont des cellules neuroendocrines, mais elles n'absorbent pas l'iode et appartiennent au système APUD.

Hormones régulées par la glande thyroïde
La glande thyroïde sécrète deux hormones contenant de l'iode - la thyroxine (T4) et la triiodothyronine (T3) et une hormone peptidique - la calcitonine. La thyroxine et la triiodothyronine (voir Hormones thyroïdiennes) se forment dans la partie apicale de l'épithélium thyroïdien, ainsi que dans l'espace intrafolliculaire, où elles s'accumulent et font partie de la thyroglobuline. La calcitonine (thyrocalcitonine) est synthétisée par les cellules C de la glande thyroïde, des glandes parathyroïdes et du thymus.
Les cellules folliculaires de la glande thyroïde sont capables de capter l'iode de la circulation sanguine qui, avec la participation de la peroxydase, se lie au colloïde de thyroglobuline. La thyroglobuline joue le rôle de réserve intrafolliculaire d'hormones thyroïdiennes. Si nécessaire, par pinocytose, une certaine quantité pénètre dans la cellule folliculaire, où, à la suite de la protéolyse, T3 et T4 sont isolés de la thyroglobuline et séparés des autres peptides iodés hormonalement inactifs.
Les hormones libres pénètrent dans le sang et les protéines iodées subissent une désiodation. L'iode libéré est envoyé pour synthétiser de nouvelles hormones thyroïdiennes. Le taux de dégradation de la thyroglobuline et la synthèse des hormones thyroïdiennes dépendent de la régulation centrale, du niveau d'iode dans le sang et de la présence de substances qui affectent le métabolisme de l'iode (globulines immunostimulantes, thiocyanates, bromures, etc.).
Ainsi, processus naturels la synthèse et la sécrétion s'effectuent à une vitesse et en quantités telles que l'organisme a besoin de maintenir un certain niveau de concentration hormonale dans les tissus, ce qui permet de maintenir l'homéostasie.
La régulation centrale est réalisée par la production de facteur de libération des hormones thyroïdiennes hormone stimulant la thyroïde) et éventuellement de la thyréostatine (un facteur qui inhibe la synthèse de l'hormone stimulant la thyroïde).
La thyréostimuline (TSH) est synthétisée par les thyrotrophes de l'hypophyse antérieure (voir Hormones hypophysaires) ; elle est responsable de la stimulation de la croissance et de l'activité fonctionnelle de l'épithélium thyroïdien. L'entrée de TSH dans le sang est régulée par le niveau de concentration d'hormones thyroïdiennes dans le sang et d'hormone de libération des hormones thyroïdiennes, mais le principal facteur régulateur est la concentration d'hormones thyroïdiennes dans le sang.
Des niveaux élevés de cette dernière rendent les thyrotrophes résistants à la thyrolibérine. La régulation périphérique du métabolisme thyroïdien dépend du nombre de récepteurs spécifiques des hormones thyroïdiennes dans la cellule ; dans des conditions de teneur élevée en hormones thyroïdiennes, leur quantité diminue considérablement; avec une faible teneur, au contraire, elle augmente. De plus, la majeure partie de la thyroxine peut être métabolisée sous une forme inactive et ainsi effectuer l'un des types de régulation périphérique de l'état fonctionnel du corps.
Le contenu physiologique des hormones thyroïdiennes est nécessaire au plein fonctionnement des processus de synthèse des protéines dans divers organes et tissus (du système nerveux central au tissu osseux) ; leur quantité excédentaire peut provoquer un découplage de la respiration tissulaire et une phosphorylation oxydative dans les mitochondries cellulaires, entraînant une forte diminution des réserves énergétiques de l’organisme.
Dans le même temps, il convient de noter qu'en augmentant la sensibilité des récepteurs aux catécholamines, les hormones thyroïdiennes provoquent une excitabilité accrue du système autonome. système nerveux, se manifestant par une tachycardie, des arythmies, une augmentation de la pression artérielle systolique, une augmentation de la motilité gastro-intestinale et de la sécrétion des sucs digestifs : ils améliorent également les processus de dégradation du glycogène, ralentissent sa synthèse dans le foie et affectent le métabolisme des lipides.
La carence en hormones thyroïdiennes provoque une forte baisse la vitesse de tous les processus oxydatifs dans le corps et l'accumulation de glycosaminoglycanes (voir Métabolisme et énergie). Les cellules du système nerveux central sont les plus sensibles à ces changements. myocarde, glandes endocrines.
Méthodes de recherche
Le diagnostic des patients présentant une pathologie thyroïdienne comprend des méthodes cliniques et de laboratoire pour évaluer son activité fonctionnelle, ainsi que des méthodes d'examen intravital (préopératoire) de la structure de la glande.
Lors de la palpation de la glande thyroïde, les spécialistes déterminent sa taille, sa consistance ainsi que la présence ou l'absence de formations nodulaires. Le plus informatif méthodes de laboratoire la détermination des hormones thyroïdiennes dans le sang est méthodes radio-immunes effectué à l’aide de kits de test standards (voir Dosage radio-immunologique).
L'état fonctionnel de la glande thyroïde est déterminé par l'absorption du pertechnétate de 131I ou 99mTc (voir Scintigraphie). Les méthodes d'évaluation intravitale de la structure de la glande thyroïde comprennent la tomodensitométrie, les diagnostics échographiques, l'analyse des radionucléides et la scintigraphie, qui fournissent des informations sur la topographie, la taille et la nature de l'accumulation du médicament radiopharmaceutique dans diverses parties de la glande, ainsi que la ponction. (aspiration) biopsie suivie d'une microscopie ponctuée.
Pathologie
Les manifestations cliniques des maladies thyroïdiennes sont causées soit par une production excessive (voir Thyrotoxicose) ou insuffisante d'hormones thyroïdiennes, soit par une production excessive de calcitonine et de prostaglandines (par exemple, dans le carcinome médullaire - une tumeur productrice de calcitonine), ainsi que par des symptômes de compression de les tissus et organes du cou de la glande thyroïde hypertrophiée sans perturbation de la production d'hormones (euthyroïdie).
Il existe cinq degrés d’hypertrophie de la glande thyroïde :
- Ô degré- la glande ne peut pas être visible lors de l'examen et ne peut être déterminée par palpation ;
- je suis diplômé- lors de la déglutition, un isthme est perceptible, qui est déterminé par la palpation, ou l'un des lobes de la glande thyroïde est palpé. et isthme ;
- IIe degré- les deux lobes sont palpés, mais à l'examen les contours du cou ne sont pas modifiés ;
- IIIe degré- la glande thyroïde est hypertrophiée à la fois au niveau des lobes et de l'isthme, perceptible lors d'une étude diagnostique et ressemble à un épaississement sur la face antérieure du cou (cou épais) ;
- IVe degré- un gros goitre, légèrement asymétrique, présente des signes de compression des tissus et organes voisins du cou ;
- V degré- un goitre extrêmement volumineux.

Défauts de développement
L'aplasie (absence) de la glande thyroïde est un phénomène rare associé à une différenciation altérée du rudiment embryonnaire du tissu thyroïdien : elle est déterminée lors du diagnostic chez les patients à un âge précoce. enfance sur la base du tableau clinique d’une hypothyroïdie congénitale sévère.
L'hypoplasie congénitale de la glande thyroïde se développe en raison d'une carence en iode dans le corps de la mère, se manifestant cliniquement par un crétinisme et un retard dans le développement physique de l'enfant. Le principal type de traitement pour les pathologies considérées est l’hormonothérapie substitutive à vie.
Lorsque le canal thyréoglosse est préservé, des kystes médians et des fistules du cou se forment souvent, ainsi qu'un goitre de la racine de la langue, qui doit être retiré. Le déplacement du rudiment thyroïdien dans le médiastin provoque le développement d'un goitre ou d'une tumeur rétrosternale. La source de leur formation peut également être des foyers de tissu thyroïdien disloqués dans la paroi de la trachée, du pharynx, du myocarde et du péricarde.
Les blessures à la glande thyroïde sont assez rares, elles sont généralement associées à des blessures à d'autres organes du cou. Plus souvent dégâts ouverts, accompagné saignements abondants, besoin urgent soins chirurgicaux. Des blessures fermées sont observées lorsque le cou est comprimé (par exemple avec un nœud coulant lorsque tentative de suicide), et des hématomes apparaissent généralement.
Maladies
Parmi les maladies de la glande thyroïde, les plus courantes sont le goitre toxique diffus et la thyroïdite auto-immune, qui sont considérées comme des maladies auto-immunes typiques avec une pathogenèse similaire, mais un tableau clinique différent, et se retrouvent souvent chez les parents par le sang.
Le groupe des maladies infectieuses et inflammatoires de la glande thyroïde associe des états pathologiques à différents symptômes cliniques, qui peuvent avoir symptômes généraux associée à la compression des tissus et des organes entourant la glande thyroïde.
Tumeurs
Les tumeurs épithéliales bénignes caractéristiques de la glande thyroïde sont des adénomes de diverses structures histologiques. La détection clinique des adénomes est possible grâce à la méthode de palpation de la glande thyroïde. Les tumeurs aux contours clairs et à la surface lisse augmentent progressivement en taille. Les ganglions lymphatiques cervicaux sont intacts et la fonction de la glande est le plus souvent inchangée.
En milieu ambulatoire en reconnaissance tumeurs bénignes en plus de la palpation, ils jouent un rôle important scintigraphie thyroïdienne, examen échographique, examen cytologique des points ponctués. Le principe principal du traitement est de réaliser une résection du lobe de la glande dans lequel la tumeur a été trouvée (hémithyroïdectomie). Le pronostic après traitement chirurgical des adénomes est favorable.
Les tumeurs malignes de la glande thyroïde sont le plus souvent représentées par diverses formes de cancer et représentent 0,5 à 2,2 % de toutes les tumeurs malignes. Autres types tumeurs malignes la glande thyroïde est un phénomène plus rare. Les maladies précancéreuses comprennent les goitres nodulaires et mixtes, ainsi que les adénomes thyroïdiens. Le cancer de la thyroïde peut se développer avec un niveau important de sécrétion d'hormone stimulant la thyroïde par l'hypophyse (généralement observée chez les patients vivant dans des régions où le goitre est endémique).
La combinaison d’irradiations externes revêt une importance particulière dans le développement du cancer de la thyroïde. zones spécifiées avec irradiation interne avec des radionucléides iodés incorporés en raison d'une contamination de l'environnement par des substances radioactives.
Manifestations cliniques du cancer de la thyroïde
Cliniquement, le cancer de la thyroïde se manifeste généralement sous deux formes. Selon les données statistiques, dans la plupart des cas, lors du diagnostic, une tumeur est détectée dans la glande thyroïde et la présence (ou l'absence) de ganglions lymphatiques régionaux (ganglions lymphatiques des sections antérolatérales du cou, supra- et zones sous-clavières, ainsi que la partie antéro-supérieure du médiastin) et les métastases à distance (poumons, os, etc.).
À la palpation, une tumeur dense, grumeleuse et souvent peu mobile est notée dans la glande, ce qui, avec le temps, entraîne une modification de la voix, une altération de la respiration ou de la fonction de déglutition.


Dans la deuxième variante clinique, la tumeur, en raison de sa petite taille, n'est pas détectée par palpation, ni par les méthodes radionucléides et échographiques (« cancer caché » de la glande thyroïde) ; Les métastases apparaissent généralement d’abord dans les ganglions lymphatiques régionaux et/ou dans les organes distants. On distingue particulièrement le cancer folliculaire dit bien différencié (adénome malin, struma métastatique de Langhans, adénome angioinvasif), qui, avec une structure relativement mature, présente une croissance invasive et la capacité de métastaser.
Diagnostic et traitement du cancer de la thyroïde
Le diagnostic du cancer de la thyroïde est extrêmement difficile en présence d'un goitre ou d'un adénome au long cours, dont les principaux signes de malignité sont leur augmentation rapide, leur épaississement, l'apparition d'une tubérosité, puis un déplacement limité de la glande.
Le diagnostic final n'est établi que par un examen cytologique ou histologique. En cas de « cancer caché », outre la détermination du taux de calcitonine (cancer médullaire), l'étape finale du diagnostic consiste souvent en une large exposition et une inspection de la glande thyroïde.
Le diagnostic différentiel des tumeurs thyroïdiennes repose sur des données cliniques et radiologiques, des résultats d'analyse de la glande, une échographie de la glande thyroïde, dont les résultats sont comparés à la norme, ainsi qu'une tomodensitométrie, une ponction ciblée de la tumeur et une cytologie ultérieure. examen de la piqûre.
Traitement chirurgical comprenant une hémithyroïdectomie, une résection subtotale de la glande thyroïde et une thyroïdectomie. En présence de métastases régionales au niveau du cou, le chirurgien doit réaliser une excision de la gaine fasciale des tissus du cou. En présence de métastases à distance d'un cancer localement résécable, une thyroïdectomie suivie d'un traitement à l'iode radioactif est indiquée.
Un pronostic favorable est possible pour les formes différenciées de cancer (folliculaire et papillaire) et défavorable pour les autres formes. La prévention du cancer de la thyroïde vise principalement à traiter le goitre et les tumeurs bénignes, à éviter l'irradiation aux rayons X et la radiothérapie de la glande thyroïde chez les enfants et les adolescents et à empêcher les radionucléides iodés de pénétrer dans l'organisme avec des aliments et des liquides.
Dans la détection précoce du cancer de la thyroïde, un rôle important est accordé à l'examen médical des patients atteints de diverses formes de goitre et à leur traitement chirurgical, ainsi qu'à l'examen des parents sanguins des patients présentant des symptômes de cancer médullaire de la thyroïde, en particulier en cas de syndrome de Sipple. et syndrome du névrome des muqueuses associé à une adénomatose des glandes endocrines.
Pour effectuer des opérations sur la glande thyroïde, une anesthésie locale ou une anesthésie par intubation est utilisée. Les patients atteints de thyréotoxicose nécessitent une préparation préopératoire spéciale avant la chirurgie.
L'accès le plus pratique à la glande thyroïde est une incision transversale arquée le long de la surface antérieure du cou, 1 à 1,5 cm au-dessus de l'encoche jugulaire. Les formes rétrosternales de goitre peuvent généralement être éliminées par cet accès, mais parfois le chirurgien doit recourir, comme chez les patients atteints de goitre intrathoracique, à une thoracotomie.
Les principales caractéristiques de chaque opération sur la glande thyroïde sont le volume d'intervention et la méthode (méthode) de résection du tissu thyroïdien. Il existe des méthodes intracapsulaires, intrafasciales et extrafasciales.
Méthode intracapsulaire le plus souvent utilisé pour l'énucléation des ganglions thyroïdiens afin de maximiser la préservation du tissu glandulaire inchangé.
Libération intrafasciale La glande thyroïde est utilisée pour toutes les formes de goitre, alors qu'il n'y a pas de traumatisme possible aux branches des nerfs laryngés récurrents et des glandes parathyroïdes, qui sont situées à l'extérieur (moins souvent à l'intérieur) de la couche viscérale du 4ème fascia du cou, sont conservés, dans lesquels l'opération est effectuée. Parfois, cette méthode est complétée par une ligature des artères sur toute la longueur.
Méthode extrafasciale est utilisé exclusivement dans la pratique oncologique et, en règle générale, implique la ligature des principales artères de la glande thyroïde.
L'étendue de l'intervention chirurgicale dépend de la nature et de la localisation du processus pathologique, de la taille du foyer pathologique et de la quantité de tissu restant. Les plus couramment utilisées sont la résection partielle, sous-totale et l'extirpation (ablation complète) d'un ou des deux lobes de la glande thyroïde.
La résection partielle est utilisée pour les petits goitres bénins nodulaires, préservant environ la moitié du ou des lobes réséqués. La résection subtotale consiste à laisser 4 à 8 g de tissu glandulaire dans chaque lobe (généralement sur la surface latérale de la trachée, dans la zone où se trouvent les nerfs laryngés récurrents et les glandes parathyroïdes).
De telles manipulations sont effectuées pour toutes les formes de goitre chez les patients atteints de thyréotoxicose, ainsi que pour les goitres euthyroïdiens nodulaires et multinodulaires, occupant presque tout le(s) lobe(s) de la glande thyroïde.
Extirpation utilisé, en règle générale, pour les néoplasmes malins de la glande thyroïde, cette opération peut être complété, selon le stade et la localisation du processus, par l'ablation des muscles adjacents à la glande, de la veine jugulaire externe et interne avec le tissu contenant les ganglions lymphatiques.
Parmi les complications possibles qui se développent après une intervention chirurgicale sur la glande thyroïde, il convient de noter la parésie des nerfs laryngés récurrents, l'hypoparathyroïdie, les saignements secondaires au début période postopératoire.
Gland est le nom de ceci organe endocrinien est en hausse ces derniers temps. Cela est dû aux tristes statistiques sur la propagation des maladies thyroïdiennes. Dans cet article, nous vous présenterons en détail l’importance de cet organe, les symptômes alarmants de ses « problèmes », une transcription de l’examen histologique et bien plus encore.
Qu'est-ce que la glande thyroïde ?
La glande thyroïde est un organe de sécrétion interne, une partie importante du système endocrinien de l'organisme. Sa tâche est la synthèse des hormones qui maintiennent l'homéostasie dans le corps. Il produit notamment des éléments contenant de l’iode, responsables de la croissance cellulaire et du métabolisme de l’organisme. Mais nous en reparlerons plus tard sur les fonctions et les hormones de la glande thyroïde.
La masse de l'organe est de 20 à 65 g. Cela dépend de l'âge de la personne - sa taille varie considérablement. Par exemple, pendant la puberté, son volume et son poids augmentent considérablement. Et avec la vieillesse, le fer commence au contraire à diminuer. Chez la femme, la glande thyroïde peut augmenter de volume pendant la grossesse et 1 à 2 ans après l'accouchement.
Structure des organes
La structure de la glande thyroïde ressemble à un papillon déployant ses ailes. L'organe est symétrique - se compose de deux lobes et d'un isthme entre eux. Les lobes sont situés de chaque côté de la trachée et l'isthme lui est adjacent.
La localisation et la structure de la glande thyroïde sont différentes selon les deux sexes :
- Chez la femme : légèrement plus grande que chez l'homme, mais le tissu adipeux sous-cutané qui protège l'organe est également plus gros, c'est pourquoi la « glande thyroïde » dans la moitié féminine est moins visible. Localisation : antérieure et latérale par rapport au cartilage thyroïde et cricoïde.
- Chez l'homme : situé juste en dessous des cartilages nommés, atteignant dans certains cas le sternum.
Le rôle de la glande thyroïde dans le corps
En parlant d'hormones et des fonctions de la glande thyroïde, la première chose que nous devons souligner est sa tâche la plus importante : l'organe produit des hormones qui fournissent échange normal substances, bon fonctionnement du cœur et du tractus gastro-intestinal. L'activité de la glande elle-même est affectée par le niveau d'iode dans le corps.

La glande thyroïde aide également l’organisme à remplir les fonctions vitales suivantes :
- Ajustement de la fréquence cardiaque et de la respiration.
- Assurer le fonctionnement normal du système nerveux - central et périphérique.
- Maintenir un poids corporel approprié.
- Fréquence des cycles menstruels.
- Température corporelle normale.
- Niveau non critique de cholestérol dans le sang.
- Régulation de la consommation d'oxygène par les cellules. Par conséquent, lorsque les fonctions d'un organe sont altérées, un plus petit volume d'oxygène pénètre dans les cellules, c'est pourquoi les radicaux libres commencent à s'y accumuler, ce qui provoque une sensation fatigue constante, provoque le développement d’autres maladies.
Hormones produites par la glande thyroïde
Plus précisément, la glande thyroïde produit trois hormones :
- T4 - thyroxine. Sa fonction : absorption des acides gras essentiels par l'organisme et métabolisme des graisses. Ralentir métabolisme des graisses entraîne une augmentation du taux de cholestérol.
- T3 - triiodothyronine. 20 % de cette hormone dans l’organisme est produite directement par la glande thyroïde, le reste est produit par des dérivés T4. Régulation du métabolisme et de l'activité cellulaire.
- impliqué dans la régulation de la proportion requise de calcium dans l’organisme.
Causes des maladies des organes
Il existe plusieurs raisons pour lesquelles la maladie se développe et, par conséquent, une histologie de la glande thyroïde est requise :

- Inflammation de l'organe lui-même.
- Niveau d’iode insuffisant/excessif dans le corps.
- Conséquence des actes médicaux : intervention chirurgicale, radiothérapie, prise de nombreux médicaments.
- Dysfonctionnement du système immunitaire.
- Grossesse. Les maladies elles-mêmes sont « lourdes » du fait qu'elles peuvent conduire à une fausse couche, naissance prématurée ou pour mortinatalité bébé.
Symptômes alarmants
Les symptômes généraux typiques des problèmes de thyroïde sont les suivants :
- Léthargie, distraction, fatigue, troubles de la mémoire, capacité de concentration.
- Perte de poids.
- Dysfonction sexuelle, déséquilibre hormonal.
- Constipation.
- Douleurs musculaires, membres constamment gelés.
- Ongles cassants, cheveux ternes et qui tombent.
- Aux yeux d'insecte.
- Rythme cardiaque augmenté.
- Agrandissement visuel de l'organe.
Maladies « thyroïdiennes »
Il existe plusieurs maladies de gravité variable, que l'histologie thyroïdienne aidera également à reconnaître.
Hyperthyroïdie. L'organe produit des quantités excessives d'hormones. Le patient atteint de cette maladie ressent et observe :
- nervosité;
- intolérance à la chaleur;
- fatigue constante;
- transpiration;
- perte de poids;
- démangeaisons cutanées;
- rythme cardiaque augmenté;
- chute de cheveux.
Hypothyroïdie. La glande produit des quantités insuffisantes d’hormones. La maladie disparaît souvent forme cachée- le malade ne le sait pas depuis des années. Elle est révélée par un type de diagnostic simple : un test de dépistage T4. Les symptômes sont les suivants :
- dépression constante;
- fatigabilité rapide;
- chute de cheveux;
- sensibilité au froid;
- peau sèche;
- les femmes ont des règles irrégulières.

Goitre. Gonflement de la glande, dont la cause est un manque d'iode dans le corps. Parfois, c'est la conséquence d'une maladie auto-immune. Les raisons peuvent être :
- l'apparition de nodules sur la glande ;
- abus de tabac;
- infections ;
- déséquilibres hormonaux ;
- radiothérapie;
- prendre des médicaments contenant du lithium.
Cancer de la thyroïde. Ce qu'il convient de noter, c'est que l'oncologie se développe ici très lentement et que les tumeurs folliculaires et papillaires sont aujourd'hui facilement traitables. Seules les tumeurs peu différenciées sont défavorables au patient - en raison de métastases actives. Pour le diagnostic, l'histologie du nodule thyroïdien est requise. Les symptômes du cancer sont les suivants :
- Une petite bosse non douloureuse apparaît sur le cou.
- Les ganglions lymphatiques du cou sont hypertrophiés.
- Douleur constante au cou et à la gorge.
- Respiration difficile.
- Voix rauque.
Diagnostique
Si des signes évoquant une maladie thyroïdienne apparaissent, vous devez consulter dès que possible un endocrinologue, qui doit d'abord prescrire un diagnostic complet, incl. analyse histologique (histologie) de la glande thyroïde.
Les méthodes de diagnostic sont divisées en méthodes physiques, de laboratoire et instrumentales. Parmi eux:
- palpation;
- test immuno-absorbant lié ;
- tomographie;
- thermographie;
- scintigraphie;
- biopsie par aspiration ;
- tests pour déterminer les niveaux de thyroxine;
- détermination de l'excrétion d'iode dans l'urine.

Nous parlerons en détail de l'examen histologique.
Histologie de la glande thyroïde
Plus correctement - une biopsie.Cette analyse vous permet de savoir si la tumeur de la «glande thyroïde» est maligne. Prescrit par un endocrinologue lorsque des nodules ou des kystes sont détectés sur un organe de plus de 1 cm de diamètre.
Si la formation est maligne, le médecin prescrit une intervention chirurgicale au patient. Cependant, cette méthode de recherche est utilisée non seulement lors du diagnostic, mais également lors d'une intervention chirurgicale, afin que le chirurgien puisse déterminer rapidement où se trouve exactement la tumeur maligne. L'histologie de la glande thyroïde est réalisée après l'opération - si tout le nécessaire a été retiré et si un nouveau est nécessaire intervention chirurgicale.

Comment se déroule l’histologie ?
Pour mener des recherches, un appareil histologique est prélevé sur le patient - un échantillon de cellules « thyroïdiennes ». Comment se déroule l’histologie de la glande thyroïde ? L’intervention est réalisée par biopsie-aspiration à l’aiguille fine, sous le contrôle d’un échographe. La procédure est indolore et prend 2 à 5 secondes.
À l'aide d'une seringue dotée d'une aiguille ultra-fine, le médecin pratique une ponction au niveau de la glande et prélève la quantité requise d'échantillon pour examen. Ensuite, le matériel est examiné sans la participation du patient.
Décoder les résultats
Bien entendu, l’interprétation de la conclusion est l’apanage d’un spécialiste expérimenté. Mais une évaluation préliminaire approximative de la glande thyroïde est également possible pour le patient :
- - une raison de se calmer. Cela signifie que l'éducation est bénigne. La précision de ce diagnostic est de 98%.
- «Épithélium folliculaire», «colloïde» - on parle aussi d'une tumeur bénigne. Précision - 95%.
- « Un ganglion présentant des symptômes de prolifération de l'épithélium folliculaire, des atypies » ou « une difficulté à différencier le carcinome et l'adénome » - nous parlons de néoplasie folliculaire. Probabilité de présence formation maligne - 50%.
- "Une malignité ne peut pas être exclue" - 70 % de probabilité de présence de cellules cancéreuses.
- « Carcinome suspecté » : probabilité de cancer de 90 %.
- Le seul mot « carcinome » signifie une probabilité de cancer des glandes presque de 100 %, la chirurgie est inévitable.
Dans tous les cas, il n'y a pas lieu de paniquer : il y a de fortes chances que le spécialiste ait commis une erreur lors de la collecte du matériel ou de la conduite des recherches. Si la conclusion indique la présence d'une tumeur maligne, l'endocrinologue oriente généralement le patient vers une nouvelle histologie.

Le traitement de la maladie thyroïdienne consiste principalement en médicaments thérapie hormonale. En cas d'échec, une intervention chirurgicale est prescrite, dont la version moderne permet de la parfaitement tolérer. En outre, lors de l'ablation de la glande ou d'une partie de celle-ci, la radiothérapie est prescrite pour les lésions cancéreuses de l'organe.
1.4. Structure histologique du tissu de la glande thyroïde inchangée
La glande thyroïde humaine (Fig. 24) a une structure lobulaire : des couches de tissu conjonctif lâche s'étendent à partir de la capsule de tissu conjonctif dense recouvrant la glande.
Figure 24. Structure microscopique de la glande thyroïde :1 – capsule ; 2 – septa interlobulaires du tissu conjonctif ; 3 – lobule ; 4 – vaisseaux sanguins interlobulaires ; 5 – capillaire sanguin ; 6 – follicule et thyrocytes folliculaires : 7 – colloïde(cité par O.V. Volkova).
tissu conjonctif fibreux - septa interlobulaires qui divisent le parenchyme en lobules. Les principaux vaisseaux – artères et veines interlobulaires – traversent les septa interlobulaires.
Les unités structurelles et fonctionnelles (adénomères) du parenchyme thyroïdien sont follicules– des formations en forme de bulles fermées, sphériques ou légèrement allongées, de différentes tailles, avec une cavité à l'intérieur (Fig. 25, 26). Leur taille moyenne est de 40 à 50 microns. S'accumule dans la lumière du follicule colloïde- un produit sécrétoire des cellules épithéliales qui constituent la muqueuse du follicule. Au cours de la vie, le colloïde est un liquide visqueux constitué principalement de thyroglobuline.

Figure 25.Structure du follicule thyroïdien(d'après Yamashita S., 1996).
Les follicules sont séparés par des couches de tissu conjonctif fibreux lâche, à travers lesquelles de nombreuses capillaires sanguins et lymphatiques, enlaçant les follicules, ainsi que les fibres nerveuses. Dans ces mêmes couches, on trouve des accumulations compactes de cellules épithéliales thyroïdiennes. De plus, les lymphocytes et les plasmocytes, ainsi que les basophiles tissulaires, se trouvent toujours dans les couches du tissu conjonctif interfolliculaire.
Dans le parenchyme de la glande thyroïde, on distingue trois types de cellules : les cellules folliculaires elles-mêmes, les cellules oxyphiles ou oncocytes (cellules d'Ashkinasi-Hürthle) et les cellules neuroendocrines parafolliculaires ou cellules C (Fig. 27).

Figure 26. Glande thyroïde inchangée: follicules de taille égale, contiennent une abondance de colloïde(d'après Yamashita S., 1996).
Endocrinocytes folliculaires, ou thyrocytes– les cellules glandulaires qui constituent l’essentiel de la paroi folliculaire et de l’épithélium extrafolliculaire. Dans les follicules, les thyrocytes forment une paroi (paroi) et sont situés en une seule couche sur la membrane basale, qui borde l'extérieur du follicule. Le colloïde qu'ils sécrètent remplit la lumière du follicule sous la forme d'une masse homogène. La fonction principale des cellules folliculaires est d'effectuer la biosynthèse et la sécrétion des hormones thyroïdiennes.
Endocrinocytes parafolliculaires ou calcitoninocytes dans le corps adulte, ils sont localisés dans la paroi des follicules, situés entre les bases des thyrocytes voisins, mais n'atteignant pas la lumière du follicule avec leur sommet (localisation intraépithéliale). De plus, des cellules parafolliculaires sont également situées dans les couches interfolliculaires du tissu conjonctif (Fig. 27). Leur nombre dans une glande normale est insignifiant - moins de 0,1 % de masse totale tissu thyroïdien. Contrairement aux thyrocytes, les cellules parafolliculaires n'absorbent pas l'iode, mais combinent la formation de neuroamines (norépinéphrine et sérotonine) avec la biosynthèse d'hormones protéiques (oligopeptides) - calcinine et somatostatine.
Régénération. Le parenchyme de la glande thyroïde est différent capacité accrueà la prolifération. La source de croissance du parenchyme thyroïdien est l'épithélium des follicules.

Figure 27. Le rapport des cellules folliculaires et parafolliculaires dans la glande thyroïde : 1 – cellule parafolliculaire (C) de localisation interfolliculaire ; 2 – cellule parafolliculaire de localisation intraépithéliale ; 3 – cellule folliculaire (A); 4 – cellule basale ; 5 – oncocyte (cellule B, cellule Ashkenazi-Hurthle) ; 6 – bourgeon épithélial, issu de la prolifération des cellules basales ; 7 – membrane basale du follicule(cité de Yu. I. Afanasv).
La division des thyrocytes entraîne une augmentation de la surface du follicule, ce qui entraîne l'apparition de plis, de saillies et de papilles faisant saillie dans la cavité des follicules. (régénération intrafolliculaire). La prolifération cellulaire peut conduire à l'apparition de bourgeons épithéliaux (Fig. 27), repoussant la membrane basale vers l'extérieur dans l'espace interfolliculaire. Au fil du temps, la biosynthèse de la thyroglobuline reprend dans les thyrocytes en prolifération de ces reins, ce qui conduit à la différenciation des îlots en microfollicules. Les microfollicules, en raison de la synthèse continue et de l'accumulation de colloïdes dans leurs cavités, augmentent en taille et deviennent identiques à ceux maternels. (régénération extrafolliculaire). Les cellules parafolliculaires ne participent pas à la folliculogenèse.
Thyroïde [glandule thyroïdienne(ANP), glandula thyréoïde(JNA, BNA)] - glande endocrine non appariée. La glande thyroïde est située dans la région antérieure du cou ; il synthétise et libère des hormones dans le sang et la lymphe qui régulent les processus de croissance, de développement, de différenciation tissulaire et de métabolisme dans le corps.
Brève description apparence La glande thyroïde a été donnée pour la première fois par K. Galen. L'orgue est décrit de manière un peu plus complète dans les travaux de A. Vesalius (1543). En 1656, T. Wharton nomma cet organe « glande thyroïde ». En 1836, King (Th. W. King) fut le premier à proposer le concept d'activité intrasécrétoire de la glande thyroïde. Baumann (E. Baumann) a noté en 1896 le lien étroit entre l'apport d'iode dans le corps et l'activité fonctionnelle de l'organe.
Anatomie comparée
La glande thyroïde des vertébrés supérieurs correspond au sillon sous-branchial de la lancette, qui s'étend ventralement le long de la ligne médiane le long de toute la partie branchiale de l'intestin. Dans les cyclostomes, la glande thyroïde est représentée par un groupe de follicules uniques situés le long de la partie crânienne de l'intestin. La glande thyroïde des sélaciens est un organe non apparié de formes diverses ; chez les amphibiens, la glande thyroïde est un organe apparié. Chez les reptiles, la glande thyroïde est presque toujours impaire, située sur la ligne médiane, près de la sortie du cœur. grands navires et, en règle générale, n'a pas de forme spécifique. Chez les oiseaux, cet organe est toujours apparié. Chez les mammifères, la glande thyroïde est située ventrale par rapport à la partie caudale du larynx et à la partie adjacente de la trachée, constituée de deux lobes reliés par un isthme chez la plupart des représentants de cette classe.
Embryologie
Le rudiment de la glande thyroïde apparaît dans l'embryon humain à la 4ème semaine développement intra-utérin(longueur de l'embryon 2,5 mm) sous la forme d'une saillie de la paroi ventrale du pharynx le long de la ligne médiane, entre les paires I et II de poches branchiales. Cette saillie est un cordon épithélial qui pousse le long de l'intestin pharyngé jusqu'au niveau de la paire III-IV de poches branchiales. Le cordon épithélial au début de son développement est le canal thyroïdien (cinctus thyroglossus) et correspond au canal excréteur de la glande thyroïde. Ensuite, l'extrémité distale du cordon épithélial bifurque et les lobes droit et gauche de la glande thyroïde se développent ensuite à partir de celle-ci. L'extrémité proximale du cordon épithélial s'atrophie et à sa place reste ensuite un reste rudimentaire - l'ouverture aveugle de la langue (foramen caecum linguae), localisée au bord du corps et à la racine de la langue. Ainsi, la glande thyroïde commence comme une glande exocrine typique et, au cours du développement ultérieur, elle devient endocrine (voir Glandes endocrines).
Les rudiments des lobes droit et gauche de la glande thyroïde, initialement compacts, augmentent rapidement de volume en raison de la prolifération de brins de cellules épithéliales, ou trabécules. Le mésenchyme avec de nombreux vaisseaux sanguins se développe entre les trabécules. Au cours de la 8e à la 9e semaine du développement intra-utérin, des follicules commencent à se former, dont la majeure partie sont des thyrocytes (cellules folliculaires, cellules A). Beaucoup moins de cellules B (cellules Askanasi) se forment dans les follicules. Les thyrocytes et les cellules B sont étroitement liés les uns aux autres. On pense que ces cellules ont des éléments souches communs ou peuvent se transformer les unes dans les autres. Au cours du développement, les dérivés de la paire V de poches branchiales se développent dans le rudiment de la glande thyroïde - les corps ultimobranchiaux, qui sont la source de cellules parafolliculaires (cellules parafolliculaires ou C) incluses dans le parenchyme de la glande thyroïde.
La glande thyroïde commence à fonctionner chez un fœtus mesurant 7 cm de long, comme en témoigne la capacité de la glande à absorber l'iode radioactif pendant cette période, ainsi que l'apparition de colloïde dans les lumières des follicules. Le fonctionnement de la glande implique la différenciation des trabécules, qui commencent à se diviser en petits follicules individuels, augmentant rapidement de volume à mesure que les colloïdes s'y accumulent.
Le poids (masse) de la glande thyroïde des nouveau-nés est en moyenne de 1 à 2 g. Dans la glande des nouveau-nés, on note une desquamation de l'épithélium folliculaire et une résorption accrue des colloïdes, ce qui est probablement dû à tension fonctionnelle glande thyroïde lors de l'adaptation aux conditions environnementales.
Anatomie
La glande thyroïde est située dans la région antérieure du cou (voir) devant et sur les côtés de la trachée (voir). Il a une forme en fer à cheval avec une concavité tournée vers l'arrière et est constitué de deux lobes de taille inégale (Fig. 1). Les lobes droit (lobus dext.) et gauche (lobus sin.) de la glande thyroïde sont reliés par un isthme non apparié (isthmus glandulae thyroïde). Dans les cas où il n’y a pas d’isthme, les deux lobes de la glande thyroïde sont vaguement adjacents l’un à l’autre.
Parfois, il existe des glandes thyroïdiennes supplémentaires (aberratives) (glandulae thyroïdeae accessoriae), soit non connectées à celle-ci, soit reliées aux lobes de la glande thyroïde par de petits cordons minces. Dans 30 à 50 % des cas, le lobe pyramidal (lobus pyramidalis) est associé à l'isthme ou au lobe gauche de la glande thyroïde, qui, en remontant, peut atteindre l'échancrure thyroïdienne supérieure du cartilage thyroïde ou le corps de l'hyoïde. os (Fig. 1).
Le poids (masse) de la glande thyroïde d'un adulte est de 20 à 60 g. La taille longitudinale de chaque lobe atteint 5 à 8 cm, la taille transversale - 2 à 4 cm, l'épaisseur - 1 à 2,5 cm. Pendant la puberté, le la glande thyroïde augmente. Ses dimensions peuvent également varier en fonction du degré d'apport sanguin ; V vieillesse la taille de la glande thyroïde diminue.
À l'extérieur, la glande thyroïde est recouverte d'une capsule fibreuse reliée par des faisceaux de tissu conjonctif au cartilage cricoïde et aux anneaux trachéaux. Les faisceaux de tissu conjonctif les plus denses forment des ligaments particuliers. Parmi eux, le ligament moyen de la glande thyroïde est particulièrement prononcé, qui s'étend de la capsule de l'isthme à la surface antérieure du cartilage cricoïde, ainsi que les ligaments latéraux droit et gauche de la glande thyroïde, situés entre la capsule de les sections inféromédiales des lobes latéraux, les surfaces latérales du cartilage cricoïde et les anneaux cartilagineux de la trachée les plus proches.

Les surfaces antérolatérales de la glande thyroïde sont recouvertes de muscles sternohyoïdiens (mm. sternohyoidei) et sternothyroïdiens (mm. sternothyroidei), les ventres supérieurs des muscles omohyoïdiens droit et gauche (mm. omohyoidei dext. et sin.), situés entre les feuilles de la plaque prétrachéale du fascia cervical. À la limite des surfaces antérolatérale et postéromédiale de la glande thyroïde, elle est adjacente à faisceau neurovasculaire cou (tsvetn. fig. 3). Le nerf laryngé récurrent (n. laryngeus recurrens) passe le long de la surface postéro-médiale de la glande thyroïde et les ganglions lymphatiques paratrachéaux sont localisés. Les surfaces postéromédiales de la glande sont adjacentes aux surfaces latérales des anneaux supérieurs de la trachée, du pharynx (voir) et de l'œsophage (voir), et en haut - aux cartilages cricoïde et thyroïdien.
L'apport sanguin s'effectue à partir des artères thyroïdiennes supérieures (aa. thyroïde sup. dext. etsi p.), s'étendant des artères carotides externes (aa. carotides ext.) et des artères thyroïdiennes inférieures (aa. thyroïde inf. dext. et sin.), s'étendant à partir des troncs thyrocervicaux (trunci thyrocervicales). Dans environ 10 % des cas, l'artère thyroïdienne inférieure (a. thyroïdea ima), qui naît du tronc brachio-céphalique (truncus brachiocephalicus) ou de la crosse aortique (arcus aortae), et moins souvent de l'artère carotide commune (a. carotis communis) participe à l’apport sanguin à la glande thyroïde. À la surface de la glande, les artères forment un réseau anastomosant (tsvetn. Fig. 4,5), qui se divise en capillaires entourant les follicules et étroitement adjacents à l'épithélium folliculaire. Le sang veineux circule à travers les veines du même nom dans la veine jugulaire interne (v. jugularis interna) et les veines brachiocéphaliques (vv. brachiocephalicae).
Le drainage lymphatique se fait par les vaisseaux lymphatiques circulant dans les ganglions lymphatiques paratrachéaux, cervicaux profonds et médiastinaux. Les capillaires lymphatiques et les petits vaisseaux lymphatiques se trouvent directement entre les follicules.
Innervation. Innervation sympathique la glande thyroïde est réalisée par des nerfs provenant de ganglions cervicaux malles sympathiques. L'innervation parasympathique est assurée par les branches du nerf vague (voir) - les nerfs laryngé supérieur (n. laryngeus sup.) et récurrent (n. laryngeus recurrens).
Histologie
À partir de la capsule fibreuse recouvrant la glande thyroïde, les septa du tissu conjonctif s'étendent profondément dans la glande, qui forment le stroma de la glande et contiennent des vaisseaux et des nerfs dans leur épaisseur. Ces septa du tissu conjonctif ne se connectent pas les uns aux autres en profondeur dans le tissu thyroïdien. Par conséquent, la division du parenchyme en lobules est incomplète et la glande est pseudo-lobulaire. La glande thyroïde a une structure histologique typique des glandes endocrines : elle ne possède pas de canaux excréteurs et chaque unité fonctionnelle est étroitement liée à système circulatoire. L'unité structurelle de la glande thyroïde est le follicule - une vésicule fermée ronde ou légèrement ovale, dont la paroi est tapissée d'épithélium sécrétoire (folliculaire).
Dans le parenchyme thyroïdien, il existe trois types de cellules (A, B et C), qui diffèrent les unes des autres tant sur le plan structurel que fonctionnel. La majeure partie des cellules du parenchyme thyroïdien sont des thyrocytes (cellules folliculaires ou cellules A), qui produisent des hormones thyroïdiennes. Selon l'état fonctionnel de la glande thyroïde, les thyrocytes peuvent être plats, cubiques ou cylindriques. Lorsque l'activité fonctionnelle de la glande thyroïde est faible, les thyrocytes sont généralement plats ; lorsque l'activité fonctionnelle de la glande thyroïde est élevée, ils sont cylindriques.
La lumière du follicule est remplie de colloïde, qui est une masse homogène colorée en rose avec de l'hématoxyline-éosine. Selon la microscopie électronique (voir), le colloïde a une structure à grains fins et une densité électronique moyenne. La majeure partie du colloïde est constituée de thyroglobuline (voir), sécrétée par les thyrocytes, dont une caractéristique est l'absorption active d'iode (voir). Le colloïde est directement adjacent à la surface apicale des thyrocytes (membrane apicale), sur laquelle se trouvent de nombreuses microvillosités. Les thyrocytes situés à proximité sont reliés entre eux au moyen de plaques d'extrémité, ou ponts terminaux, et de desmosomes. Des plis profonds peuvent apparaître sur la surface basale des thyrocytes, particulièrement prononcés pendant la période d'activité fonctionnelle, qui augmentent considérablement la surface des cellules face aux capillaires sanguins. Entre les thyrocytes et les capillaires sanguins se trouvent une membrane basale, une substance fondamentale, un mince collagène et des fibres réticulaires orientées dans des directions différentes.

Le réticulum endoplasmique granulaire est bien développé dans le cytoplasme des thyrocytes (voir Réticulum endoplasmique). Les mitochondries sont réparties dans toute la cellule, mais dans la partie apicale il y en a toujours un peu plus que dans la partie basale de la cellule. Il existe une connexion topographique claire entre les mitochondries et les tubules du réticulum endoplasmique granulaire. Ainsi, ces dernières « enveloppent » souvent les mitochondries individuelles. Dans le même temps, les mitochondries peuvent « englober » partiellement ou complètement des éléments individuels du réticulum endoplasmique. Dans les thyrocytes, le complexe de Golgi est bien développé (voir Complexe de Golgi), représenté par de grandes vacuoles, des citernes aplaties (vacuoles) et des microbulles. À l'intérieur de l'anneau du complexe de Golgi, ainsi qu'à proximité, se trouvent des granules de différentes tailles et formes et de différentes densités électroniques, qui sont révélées lors de l'administration d'iode radioactif (Fig. 2, a). Des granules similaires sont présents non seulement près du complexe de Golgi, mais également dans d’autres parties de la cellule ; par exemple, dans sa partie apicale, ils forment parfois des amas entiers, constitués de plusieurs rangées de granules (de 3 à 8), situées les unes sous les autres. En plus des granules caractéristiques, des gouttes intracellulaires de colloïde sont parfois détectées dans la partie apicale des thyrocytes.
Les cellules B (cellules Askanasi) sont plus grandes que les thyrocytes, possèdent un cytoplasme éosinophile et un noyau rond situé au centre. Ils contiennent un grand nombre de mitochondries ovales ou rondes, parmi lesquelles se trouvent des granules sécrétoires. Des amines biogènes, dont la sérotonine (voir), ont été identifiées dans le cytoplasme de ces cellules. Les cellules B apparaissent pour la première fois entre 14 et 16 ans. On les retrouve en grand nombre chez les personnes âgées de 50 à 60 ans.
Les cellules parafolliculaires (périfolliculaires, ou cellules C ou cellules K) diffèrent des thyrocytes en ce sens qu'elles n'ont pas la capacité d'absorber l'iode. Ils assurent la synthèse de la calcitonine (voir), une hormone impliquée dans le métabolisme du calcium dans l'organisme. Des cellules parafolliculaires individuelles ou des groupes de cellules sont localisées sur la surface externe des follicules (Fig. 2). Ils n'entrent jamais en contact avec le colloïde dont ils sont séparés par le cytoplasme des thyrocytes. Les cellules parafolliculaires ont une taille relativement grande et une faible densité électronique du cytoplasme, qui est densément rempli de granules protéiques, révélé par l'argenture (Fig. 2, b). Le réticulum endoplasmique granulaire et le complexe de Golgi sont bien développés dans les cellules parafolliculaires.
Outre les follicules de la glande thyroïde, on distingue des îlots interfolliculaires (extrafolliculaires), formé de cellules, dont la structure ressemble à celle des thyrocytes typiques. Au centre de certains îlots interfolliculaires se trouvent des microfollicules constitués de plusieurs cellules. Les îlots interfolliculaires comprennent également des cellules parafolliculaires. Les cellules parafolliculaires se trouvent le plus souvent dans les îlots situés dans la partie centrale de la glande, où elles représentent environ 2 à 5 % de toutes les cellules. Les îlots interfolliculaires sont importants dans la régénération du tissu thyroïdien si les dommages causés à ce dernier sont importants et s'accompagnent de la mort de follicules entiers. En cas de lésion partielle des follicules, la régénération est réalisée grâce aux thyrocytes situés à la base. Grâce à ce dernier, la régénération physiologique de l'épithélium folliculaire se produit.
Physiologie
Le rôle physiologique de la glande thyroïde est la biosynthèse et la libération dans le sang et la lymphe d'hormones qui régulent les processus de croissance, de développement, de différenciation tissulaire et activent le métabolisme dans le corps. Une caractéristique spécifique des thyrocytes est la capacité d'absorber activement, d'accumuler l'iode et de le convertir en une forme organiquement liée par la formation d'hormones thyroïdiennes contenant de l'iode - la thyroxine (voir) et la triiodothyronine (voir).
Le processus de sécrétion se produisant dans la glande thyroïde se compose de trois phases. Dans la première phase (phase de production), se produit la formation de thyroglobuline, ainsi que l'oxydation des iodures en iode atomique. Dans la deuxième phase (phase d'excrétion ou de sécrétion), la thyroglobuline est libérée dans la lumière du follicule, s'y condense sous forme de colloïde et est iodée. La troisième phase (phase d'excrétion) consiste en la réabsorption du colloïde par les thyrocytes, le transport des substances réabsorbées à travers le cytoplasme jusqu'à la partie basale du thyroïde et la libération des hormones thyroïdiennes dans le sang.
La phase de production de thyroglobuline commence par l'accumulation des premiers acides aminés provenant du sang dans le réticulum endoplasmique granulaire du thyrocyte. Sous l'influence de l'ARN messager (voir Acides ribonucléiques) contenus dans les ribosomes (voir), se produit la synthèse d'un polypeptide primaire, qui s'accumule dans les lacunes du réticulum endoplasmique. C’est là que commence l’ajout de glucides (galactose et mannose) au polypeptide. Le polypeptide primaire synthétisé se déplace vers le complexe de Golgi, où sa glycolyse est terminée et les molécules de glycoprotéine qui composent la thyroglobuline sont assemblées et conditionnées (voir). Les vésicules sécrétoires qui se forment dans la zone du complexe de Golgi et contiennent une glycoprotéine (thyroglobuline non iodée) sont déplacées vers la partie apicale du thyrocyte, fusionnent leurs membranes avec sa membrane apicale et libèrent le contenu dans la lumière du follicule par exocytose. .
L'iode pénètre dans les thyrocytes à partir du sang sous forme d'iodure (ion iode), est transporté à travers leur cytoplasme et est libéré à travers la membrane apicale dans la lumière du follicule, remplie de colloïde.
L'absorption de l'iode par les thyrocytes est considérée comme un processus actif et énergétique de transfert d'iode contre un gradient de concentration. Ce transport hautement actif et hautement spécifique de l'iode, ainsi que la conversion aiguë de cet élément en une forme liée, déterminent le rôle de la glande thyroïde en tant qu'organe principal du métabolisme de l'iode dans l'organisme (voir Métabolisme de l'iode). dans la glande thyroïde dépasse de 10 à 100 fois son niveau dans les autres tissus et le sérum sanguin.
Étant donné que seul l'iode atomique peut participer au processus d'iodation de la thyroglobuline, l'iodure subit une oxydation qui se produit dans la zone sous-apicale du cytoplasme des thyrocytes avec la participation de la peroxydase (voir Peroxydases).
La phase de libération, ou sécrétion, des hormones thyroïdiennes commence par la libération de thyroglobuline non iodée dans la lumière du follicule et son entrée dans le colloïde. L'iodation de la thyroglobuline (incorporation d'atomes d'iode dans des radicaux tyrosyle) se produit dans la zone périphérique des follicules, à la frontière de la partie apicale du thyrocyte et du colloïde. Les acides aminés qui composent le composant protéique de la molécule de thyroglobuline comprennent la tyrosine (voir) et ses dérivés - les thyronines, qui, subissant l'iodation, donnent naissance aux hormones thyroïdiennes : thyroxine (T4) et triiodothyronine (T3). Pour plus de détails sur la synthèse des hormones thyroïdiennes, voir Iodotyrosines, Iodothyronines, Thyroxine, Triiodothyronine.
Parallèlement à la thyroglobuline, la glande thyroïde produit de la thyroalbumine, qui est également iodée, mais seulement partiellement, au stade des iodotyrosines. Normalement, le rapport entre les concentrations de thyroglobuline et de thyroalbumine est d’environ 9 : 1. À conditions pathologiques, accompagnée de la prolifération du parenchyme thyroïdien, de sa transformation goitreuse et de l'apparition d'adénomes, la formation de thyroalbumine augmente et, en cas de tumeurs malignes de la glande thyroïde, elle peut même dépasser la formation de thyroglobuline. De plus, des histidines iodées et de la thyroxamine ont été trouvées dans la glande thyroïde. Tous les acides aminés iodés qui composent les protéines thyroïdiennes sont des isomères L (voir Isomérie).
La dernière (troisième) phase du processus de sécrétion se produisant dans les thyrocytes est la phase d'excrétion des hormones thyroïdiennes des follicules dans le sang. Étant donné que les hormones thyroïdiennes sont contenues dans des molécules de thyroglobuline à l'état lié, les besoins de l'organisme en elles ne peuvent être satisfaits qu'en décomposant la molécule de thyroglobuline. La phase d'excrétion s'accompagne d'une augmentation significative des processus de dissimilation des thyrocytes (comme en témoigne une nette augmentation de leur absorption d'oxygène) et d'un fort gonflement de leur cytoplasme et de leurs noyaux. La phase d'élimination commence par la réabsorption du colloïde par les thyrocytes. Des études au microscope électronique ont établi que le colloïde est réabsorbé par sa phagocytose active par les thyrocytes utilisant des pseudopodes (macroendocytose). Des gouttes de colloïde apparaissent dans le cytoplasme des thyrocytes, auxquelles les lysosomes s'approchent et fusionnent avec eux. La thyroglobuline des gouttes colloïdales est décomposée par l'action des enzymes lysosomales (voir), entraînant la libération d'iodotyrosines : monoiodotyrosine et diiodotyrosine et iodothyronines (thyroxine et triiodothyronine), qui s'accumulent dans des vacuoles et des citernes qui se déplacent vers la partie basale du thyrocyte. . Dans ce cas, les iodotyrosines sont complètement désiodées et ne pénètrent pas dans le sang, et l'iode qu'elles libèrent est à nouveau utilisée dans la biosynthèse des hormones thyroïdiennes. Une fois les vacuoles vidées, les iodothyronines pénètrent par la membrane basale et l'espace péricapillaire dans les capillaires sanguins (en partie également dans les capillaires lymphatiques) qui entrelacent le follicule.
L'apparition de pseudopodes et de gouttelettes colloïdales dans les thyrocytes n'est observée que dans période initiale phases d’élimination. Par la suite, avec une fonction thyroïdienne normale, les processus de sécrétion se déroulent sans formation accrue de pseudopodes et de gouttelettes colloïdales par pinocytose (microendocytose). Ces mécanismes entrent en vigueur de manière séquentielle : dans la période initiale de la phase d'excrétion, la macroendocytose par pseudopodes prédomine, puis elle est remplacée par la microendocytose.
La libération d'hormones thyroïdiennes dans le sang par la glande thyroïde, amenée dans un état d'hyperfonctionnement par une exposition répétée à l'hormone stimulant la thyroïde, se déroule dès le début sous la forme d'une microendocytose sans formation de pseudopodes et de gouttes bien visibles de colloïde intracellulaire. . Les mêmes ratios sont déterminés dans la thyréotoxicose (voir), lorsqu'un taux élevé de thyroxine et de triiodothyronine dans le sang indique non seulement une augmentation de la production d'hormones thyroïdiennes, mais également leur excrétion intensive dans le sang ; dans ce cas, ni les pseudopodes ni les gouttes claires de colloïde intracellulaire ne sont détectés.
En plus des hormones thyroïdiennes iodées, la glande thyroïde produit de la calcitonine (voir), une hormone protéique sans iode qui réduit les taux de calcium dans le sang. La calcitonine est produite par les cellules parafolliculaires. Les cellules parafolliculaires sont d'origine modifiée cellules nerveuses(neuroendocrinien) et conservent la capacité d'absorber les précurseurs des neuroamines (L-DOPA et 5-hydroxytryptophane) et de les décarboxyler, respectivement, en nor-adrénaline (voir) et en sérotonine. La teneur élevée en neuroamines et la capacité à produire des hormones protéiques déterminent l'inclusion des cellules parafolliculaires de la glande thyroïde dans le système APUD (voir Système APUD). Les cellules parafolliculaires potentialisent l'activité de l'épithélium folliculaire et aident à maintenir l'homéostasie intra-organique de la glande thyroïde.
La fonction des cellules B est déterminée par l'accumulation d'amines biogènes, notamment la sérotonine, et la potentialisation de l'activité physiologique de l'épithélium folliculaire.
Régulation de la sécrétion d'hormones thyroïdiennes
L'hormone stimulant la thyroïde de l'hypophyse est considérée comme un stimulateur spécifique de la glande thyroïde. La fonction de stimulation de la thyroïde de l'hypophyse antérieure, à son tour, est activée par la thyrolibérine sécrétée par l'hypothalamus (voir Neurohormones hypothalamiques). Par conséquent, les dommages à l'hypothalamus entraînent le même affaiblissement de la glande thyroïde que l'hypophysectomie (voir Glande pituitaire). Cette méthode de régulation peut être désignée comme transadénopituitaire.
À leur tour, les hormones thyroïdiennes (en particulier la triiodothyronine) inhibent la fonction stimulant la thyroïde de l'hypophyse (et, vraisemblablement, la sécrétion de thyrolibérine par l'hypothalamus), c'est-à-dire la relation entre l'activité fonctionnelle de la glande thyroïde et l'intensité de la fonction stimulant la thyroïde de l'hypophyse représente un système de rétroaction négative (voir), assurant la préservation des fluctuations de l'activité fonctionnelle de la glande thyroïde dans les limites de la norme physiologique.
L'hormone stimulant la thyroïde, qui pénètre dans la glande thyroïde par la circulation sanguine, est perçue par des récepteurs spécifiques localisés dans la membrane plasmique des thyrocytes. Ces récepteurs, lorsqu'ils sont combinés à l'hormone stimulant la thyroïde, activent le système adénylate cyclase des thyrocytes, qui, par l'intermédiaire de l'adénosine monophosphate cyclique (AMPc), active systèmes enzymatiques thyrocytes, ce qui augmente leur activité fonctionnelle.
Il a été établi que la sécrétion d'hormones thyroïdiennes est activée directement par des impulsions sympathiques, mais pas aussi intensément que par l'hormone stimulant la thyroïde. Les impulsions parasympathiques provoquent l'inhibition de ces processus. Ainsi, les influences régulatrices de l'hypothalamus (voir) sur la glande thyroïde peuvent se produire à la fois par l'hypophyse et en la contournant (parapituitaire).
Dans le même temps, les signaux afférents de la glande thyroïde, arrivant le long des voies nerveuses centripètes, atteignant l'hypothalamus, affaiblissent la fonction de stimulation thyroïdienne de l'hypophyse ; par conséquent, une rétroaction négative entre la glande thyroïde et l'hypophyse se manifeste également par action directe impulsions nerveuses. L'état et l'activité des cellules parafolliculaires de la glande thyroïde ne dépendent pas de l'hypophyse et ne sont pas perturbés après une hypophysectomie ; leur fonction est stimulée par des impulsions sympathiques et les impulsions parasympathiques sont inhibées. Dans le même temps, l'activité sécrétoire des cellules parafolliculaires dépend directement de la concentration de calcium dans le sang : une augmentation ou une diminution de celle-ci entraîne une augmentation ou une diminution correspondante de la sécrétion de calcitonine par les cellules parafolliculaires. En interagissant de manière antagoniste avec l'hormone parathyroïdienne (voir Hormone parathyroïdienne) des glandes parathyroïdes (voir Glandes parathyroïdes), la calcitonine garantit que le niveau de calcium dans l'organisme reste constant.
Métabolisme des hormones thyroïdiennes dans le corps
Presque toute la thyroxine entrant dans le sang est liée de manière réversible aux protéines sériques, principalement avec la L-globuline - ce qu'on appelle la globuline liant la thyroxine, et en partie avec la préalbumine et l'albumine liant la thyroxine. Par conséquent, la concentration d'iode lié aux protéines (voir) dans le sang est souvent considérée comme un indicateur de l'activité sécrétoire de la glande thyroïde. La liaison de la thyroxine aux protéines sériques empêche sa destruction, mais empêche son effet actif sur les cellules. Un équilibre dynamique s'établit entre la thyroxine liée et la thyroxine libre dans le sang, et seule la thyroxine libre a un effet sur les cellules et les tissus en réaction. La triiodothyronine se lie moins facilement aux protéines sériques que la thyroxine. La demi-vie de la thyroxine dans le sang dure 6 à 7 jours, la triiodothyronine se décompose plus rapidement (demi-vie 2 jours).
La réception de la thyroxine se produit à l'intérieur des cellules. Après avoir pénétré dans la cellule, la thyroxine perd immédiatement un atome d'iode et se transforme en triiodothyronine. Le point d'application de la triiodothyronine (à la fois reçue du sang et formée à partir de la thyroxine) est l'ADN, où la triiodothyronine stimule la transcription (voir) et la formation d'ARN.
Dans les cellules, une désiodation supplémentaire de la thyroxine et de la triiodothyronine, une désamination, un clivage de la liaison diphényléther et une décarboxylation se produisent (voir Métabolisme de l'iode).
Dans le métabolisme des hormones thyroïdiennes, le rôle principal est joué par le foie, dans lequel les produits de dégradation des iodothyronines désiodées sont liés en conjugués glucuroniques et soufrés, puis pénètrent dans les intestins avec la bile, d'où l'iode libéré est réabsorbé dans le sang. , transféré à la glande thyroïde et réutilisé.
Le rôle des hormones thyroïdiennes dans la morphogenèse et la régulation des processus physiologiques
Les effets provoqués par les hormones thyroïdiennes reposent sur leur influence sur l’absorption de l’oxygène et les processus oxydatifs dans le corps. Il a été établi que la thyroxine à doses toxiques agit sur les mitochondries cellulaires, découplant la synthèse d'ATP du transfert d'électrons le long de la chaîne respiratoire et bloquant ainsi la phosphorylation oxydative (voir).
Les hormones thyroïdiennes augmentent la production de chaleur et, en cas de carence (hypothyroïdie), la température corporelle diminue. Parallèlement, l'hypothyroïdie (voir) s'accompagne d'une rétention d'eau dans l'organisme et d'une diminution de l'excrétion de calcium et de phosphore dans les urines.
Les hormones thyroïdiennes augmentent la dégradation du glycogène (voir) et réduisent sa formation dans le foie. Le déficit de ces hormones s'accompagne d'un dérégulation le métabolisme des glucides(voir) et augmenter la tolérance du corps au glucose. En cas d'hyperthyroïdie (voir Thyrotoxicose), l'excrétion d'azote dans l'urine augmente et la phosphorylation de la créatine (voir) est altérée. Dans des conditions d'hypothyroïdie, la teneur en cholestérol (voir) dans le sang augmente et avec un excès d'hormones thyroïdiennes , son niveau diminue. Dans le même temps, avec l'hyperthyroïdie, l'excitabilité du système nerveux supérieur (en particulier son département sympathique) augmente, ce qui se manifeste par une tachycardie (voir), des arythmies (voir Arythmies cardiaques), une augmentation de la vitesse du flux sanguin, une augmentation de la pression artérielle systolique. Dans le même temps, la motilité du tractus gastro-intestinal et la sécrétion des sucs digestifs augmentent.
Les hormones thyroïdiennes sont nécessaires au fonctionnement normal du système nerveux central. L'insuffisance des hormones thyroïdiennes pendant la période embryonnaire et au début de la période postnatale peut entraîner un retard dans la différenciation du cortex cérébral et le développement mental de l'enfant, pouvant aller jusqu'au crétinisme (voir).
Les hormones thyroïdiennes, ainsi que l'hormone somatotrope (voir), participent à la régulation de la croissance corporelle (stimulent notamment l'ossification).
Caractéristiques de la fonction thyroïdienne pendant les périodes prénatales et postnatales
Pendant la grossesse, l'activité fonctionnelle de la glande thyroïde de la mère augmente ; Une augmentation du taux de thyroxine totale dans le sang est associée à une synthèse accrue de l'hormone stimulant la thyroïde sous l'influence des œstrogènes placentaires.
La capacité de la glande thyroïde à concentrer et à accumuler l'iode apparaît chez le fœtus à 10-12 semaines de développement intra-utérin. Dans le même temps, commence la synthèse de la monoiodothyronine, de la diiodothyronine, de la triiodothyronine, de la thyroxine et de la globuline liant la thyroxine. La thyrolibérine (thyrolibérine) et la thyréostimuline apparaissent dans le sérum sanguin fœtal (voir). origine hypophysaire. Les relations régulatrices entre la thyréostimuline et les hormones thyroïdiennes s'établissent à partir de la 30ème semaine de développement intra-utérin.
Aucun parallélisme n'a été détecté entre la teneur en hormones thyroïdiennes et thyroïdiennes dans le sang de la mère et du fœtus, puisque le transport transplacentaire de ces hormones est inférieur à 1 %. Concentration la plus élevée les hormones thyroïdiennes pendant la période prénatale sont détectées chez le fœtus avant sa naissance.
Immédiatement après la naissance, il y a une période d'activité fonctionnelle accrue de la glande thyroïde. Le niveau d'hormone stimulant la thyroïde augmente 30 minutes après la naissance et après 24 à 48 heures, il diminue au même niveau que chez les adultes. La teneur en triiodothyronine augmente au maximum à la fin du premier jour. L'augmentation maximale de la teneur en thyroxine est observée 24 à 48 heures après la naissance, puis une diminution progressive de son niveau se produit.
Chez les bébés prématurés (voir), l'augmentation de la teneur en hormone stimulant la thyroïde et en hormones thyroïdiennes est moins prononcée, en particulier chez les enfants de faible poids à la naissance. Cependant, quelques semaines après la naissance, ces bébés connaissent une diminution des taux d’hormones thyroïdiennes, tout comme les bébés nés à terme. Chez les bébés nés à terme ou prématurés atteints de diverses maladies, le niveau d'hormones thyroïdiennes et d'hormones thyroïdiennes peut être considérablement réduit, mais en quelques semaines, il revient à la normale.
Modifications liées à l'âge dans l'activité fonctionnelle de la glande thyroïde
L'activité fonctionnelle de la glande thyroïde reste longtemps à un niveau stable. Ce n'est qu'à un âge avancé que l'on observe des modifications atrophiques du parenchyme de la glande, accompagnées d'une légère diminution du niveau du métabolisme général, mais il existe des signes d'activité fonctionnelle accrue de la glande thyroïde, qui peuvent être considérées comme une réaction compensatoire qui contrecarre l'affaiblissement des processus oxydatifs dans les tissus d'un organisme vieillissant.
Anatomie pathologique
La dystrophie peut être observée en cas de troubles du métabolisme tissulaire (cellulaire) de la glande thyroïde, principalement dans des conditions pathologiques. Des types tels que la dystrophie thyroïdienne granulaire (parenchymateuse) et hydropique (voir Dystrophie vacuolaire) sont des types de dystrophie protéique (voir). Avec la dystrophie granulaire, des inclusions de nature protéique apparaissent dans le cytoplasme des thyrocytes, un gonflement des mitochondries, un aplatissement de leurs crêtes sont notés, une expansion des citernes du réticulum endoplasmique est détectée et une accumulation de protéines dans celles-ci. Avec la dystrophie hydropique, des vacuoles remplies de liquide apparaissent dans le cytoplasme des thyrocytes, moins souvent dans le noyau.
L'amylose de la glande thyroïde est rare. Elle est observée dans l'amylose généralisée (voir) et se caractérise par le dépôt d'amyloïde dans le stroma de la glande, la membrane basale des follicules et les parois des vaisseaux sanguins et lymphatiques. Les dépôts amyloïdes sont caractéristiques du cancer médullaire de la thyroïde. La participation des cellules épithéliales tumorales à la formation de l’amyloïde a été prouvée.
Le remplacement du parenchyme thyroïdien par du tissu adipeux est observé avec une atrophie de la glande thyroïde, notamment avec ce qu'on appelle l'atrophie hormonale, accompagnée d'une diminution de la fonction glandulaire, par exemple avec un apituitarisme (voir), un myxœdème (voir). Un remplacement congénital complet de la glande thyroïde par du tissu adipeux a également été décrit.
Les dystrophies minérales de la glande thyroïde (calcinose) peuvent être intracellulaires et extracellulaires, caractérisées par la précipitation de sels de calcium sous forme de grains de différentes tailles dans des cellules et structures nécrotiques ou dystrophiquement altérées. La matrice de calcification intracellulaire est constituée de mitochondries et de lysosomes de thyrocytes, et la matrice extracellulaire (la plus courante) est constituée de fibres de collagène du stroma. La cause de la calcification est constituée de facteurs locaux, ainsi que de facteurs généraux, tels que l'hypercalcémie (voir), qui survient avec un manque de calcitonine (voir), avec une hyperproduction d'hormone parathyroïdienne (voir), une libération accrue de calcium du dépôt et diminution de l'excrétion de calcium du corps.
Des perturbations du métabolisme des pigments de la glande thyroïde, notamment hémoglobinogènes, sont observées dans les zones d'hémorragie lors de l'hémosidérose (voir) et de l'hémochromatose (voir). Dans ce cas, l'hémosidérine et la ferritine se trouvent le long des fibres stromales, dans le cytoplasme des cellules.
La nécrose du tissu thyroïdien sous forme d'infarctus ischémique (voir) se développe avec la ligature des artères thyroïdiennes ou leur thrombose, avec l'athérosclérose (voir), les néoplasmes des organes du cou. Une nécrose mineure de la glande thyroïde est observée avec diverses options goitre (voir), avec thyroïdite (voir), due à des troubles circulatoires, avec irradiation (voir).
Les troubles circulatoires se manifestent par des troubles de l'apport sanguin à la glande thyroïde, une thrombose de ses vaisseaux, une embolie et une crise cardiaque. L'hyperémie collatérale est le plus souvent observée (lorsque le flux sanguin est obstrué en raison d'une hyperplasie du tissu thyroïdien ou de la croissance de sa tumeur). La stagnation prolongée du sang dans la glande thyroïde entraîne la mort de son parenchyme et s'accompagne d'une sclérose acellulaire. Une conséquence des troubles hémodynamiques observés au cours traumatisme à la naissance, l'hypertension artérielle, la vascularite systémique, les maladies infectieuses (typhoïde, septicémie), la leucémie, l'anémie, sont des hémorragies (voir), des plasmorragies (voir). Une plasmorragie dans la glande thyroïde est observée lorsque la perméabilité des vaisseaux microvasculaires est altérée (voir Microcirculation). Au microscope, on note un aplatissement de l'endothélium vasculaire, un gonflement fibrinoïde (voir Transformation fibrinoïde) et une nécrose de la paroi vasculaire.
L'inflammation de la glande thyroïde est rare ; peut survenir avec une amygdalite, une ostéomyélite, une septicémie, ainsi qu'avec certains maladies infectieuses(par exemple, tuberculose, syphilis, actinomycose). Cela peut survenir de manière aiguë, subaiguë et chronique. La thyroïdite purulente aiguë se caractérise par la formation d'abcès petits ou grands dans la glande thyroïde. Les gros abcès peuvent se rompre dans le médiastin, la trachée et à travers la peau pour former des fistules. Les thyroïdites spécifiques (tuberculeuses, syphilitiques, actinomycose) sont rares, généralement en tant que manifestation maladie générale(voir Thyroïdite).
Des kystes de différentes tailles se trouvent le plus souvent dans la glande thyroïde goitreuse ; ils surviennent en conséquence anciennes hémorragies et la stase colloïdale ( kystes folliculaires), ainsi qu'à la suite d'une malformation des corps ultimobranchiaux (kystes ultimobranchiaux). Les kystes (voir Kyste), en particulier les folliculaires, sont tapissés d'un épithélium cubique ou pavimenteux et ont une paroi fibreuse épaissie.
L'atrophie de la glande thyroïde est observée chez les personnes âgées, parfois accompagnées de diabète sucré, d'hypovitaminose B, d'hyperplasie surrénalienne, de maladies de l'hypophyse, etc. On distingue l'atrophie primaire ou idiopathique de la glande thyroïde et l'atrophie résultant d'une thyroïdite auto-immune. . L'atrophie de la glande thyroïde se caractérise par une diminution de son poids (masse), du nombre et de la taille des follicules et des cellules. L'atrophie du parenchyme thyroïdien peut s'accompagner du remplacement du tissu glandulaire par du tissu conjonctif. Parfois, dans les foyers de sclérose, il existe une métaplasie (voir) des thyrocytes cylindriques en thyrocytes plats (métaplasie épidermoïde).
L'hyperplasie du tissu thyroïdien pendant la puberté (voir) est associée à des modifications de la fonction des gonades. Dans des conditions pathologiques, l'hyperplasie (voir) est causée par une sécrétion excessive d'hormone stimulant la thyroïde par l'hypophyse. Elle peut être diffuse et focale. Avec l'hyperplasie, il y a une prolifération accrue des cellules des îlots interfolliculaires avec la formation de nouveaux follicules et thyrocytes, formant des processus papillaires et ce qu'on appelle les oreillers de Sanderson (voir Goitre sporadique). Il y a une augmentation de la hauteur des thyrocytes, une accumulation de ribonucléoprotéines, d'iodure peroxydase dans la zone périnucléaire et de thyroglobuline dans les parties apicales de la cellule. Caractérisé par une augmentation de la taille des noyaux, du nombre et de la taille des organites cytoplasmiques. Une hyperplasie des structures fibrillaires de la membrane basale des follicules et des capillaires sanguins est révélée. Dans les follicules, une liquéfaction et une résorption accrue du colloïde peuvent être observées (avec goitre toxique diffus).
Méthodes d'examen
Les méthodes d'examen des patients atteints de maladies thyroïdiennes comprennent Examen clinique et des méthodes d'évaluation de la fonction et de la structure de la thyroïde.
L'examen clinique est un maillon important dans le diagnostic des maladies thyroïdiennes. Il s'agit de recueillir des plaintes, des anamnèses et des données objectives (état de la peau, des tissus sous-cutanés, capillaires, neuromusculaires et neuromusculaires). systèmes cardiovasculaires, tube digestif). Une attention particulière est portée à la palpation de la glande thyroïde, qui renseigne sur la taille, la symétrie des lobes et la consistance de l'organe.
La fonction thyroïdienne est évaluée à l'aide de méthodes indirectes et spécifiques. Les méthodes indirectes sont basées sur la recherche fonctions physiologiques organismes qui sont influencés par les hormones thyroïdiennes. Les indicateurs obtenus à l'aide de ces méthodes ne sont pas spécifiques à la pathologie thyroïdienne, car des changements similaires peuvent également survenir dans les maladies d'autres organes. Les méthodes indirectes comprennent l'étude du métabolisme basal (voir Métabolisme et énergie), des graisses (la teneur en cholestérol et en acides gras non estérifiés dans le sang) et du métabolisme protéique, de l'état du système neuromusculaire (voir Réflexométrie) et cardiovasculaire (voir Électrocardiographie). systèmes.
Les méthodes spécifiques d'évaluation de l'état fonctionnel de la glande thyroïde comprennent des études sur le niveau d'hormones thyroïdiennes dans le sang et le métabolisme de l'iode (voir Métabolisme de l'iode). Pour déterminer les hormones thyroïdiennes, utilisez diverses méthodes, y compris les biochimiques. Ces derniers permettent d'établir la concentration dans le sang de l'iode lié par les protéines plasmatiques (voir Iode lié aux protéines) et de l'iode extrait par le butanol (voir Iode extractible au butanol). Les méthodes chimiques de détermination des hormones thyroïdiennes demandent beaucoup de travail et sont complexes. Avec l'introduction des méthodes immunologiques, elles ont perdu de leur importance et ne sont utilisées que dans des laboratoires spécialisés.
Les méthodes immunologiques reposent sur le principe de la liaison compétitive des hormones et d'autres substances testées par des anticorps spécifiques. Un radionucléide est utilisé comme marqueur (voir Méthode radioimmunologique). Actuellement, ces méthodes sont utilisées pour déterminer le total et thyroxine gratuite(T4), total, libre et inverse, ou inverse, triiodothyronine (T3), globuline liant la thyroxine (TBG), hormone stimulant la thyroïde (TSH), thyrolibérine (TRH) et anticorps contre la thyroglobuline. La recherche est effectuée in vitro à l'aide de kits de tests spéciaux selon des méthodes standard.
Les méthodes spécifiques d'évaluation du métabolisme de l'iode comprennent également les méthodes radionucléides utilisant le pertechnétate de 123 I, 125 I, 131 I, 132 I et 99m Tc (voir Produits radiopharmaceutiques). Contre-indications absolues il n'existe pas d'utilisation de ces radionucléides ; les radionucléides relatifs incluent l'enfance, la grossesse et l'allaitement, et lors de l'utilisation d'iode radioactif, une fonction thyroïdienne réduite. 1,5 à 2 mois avant l'étude, tous les médicaments contenant de l'iode et du brome, les antithyroïdiens, les sédatifs, les hormones, l'introduction de composés iodés radio-opaques et la lubrification de la peau avec une solution alcoolique d'iode sont arrêtés ; Les produits riches en iode (algues et poissons, eaux minérales, kakis, etc.) sont exclus de l'alimentation. Pour étudier le métabolisme intrathyroïdien de l'iode, un test d'accumulation d'iode radioactif et de 99tTs-pertech-nétate par la glande thyroïde est utilisé. Pour ce faire, le patient reçoit par voie orale ou intraveineuse 0,0025-0,005 µCurie (0,1-0,2 MBq) 131 I, 125 I ou 0,001-0,02 µCurie (0,4-0,8 MBq) 123 I, 132 I ou 1 microcurie (40 MBq) Pertechnétate de 99m Tc. Le rayonnement gamma est enregistré à l'aide d'une installation radiométrique monocanal dont le capteur est situé à 25-30 cm de la surface antérieure du cou du patient. L'intensité du rayonnement sur la glande thyroïde est enregistrée 2, 4 et 24 heures après la prise ou l'administration du radionucléide. Les résultats radiométriques obtenus (voir) sont comparés à l'activité totale du radionucléide introduit dans l'organisme, prise à 100 %. Chez les individus sains, l'accumulation d'iode radioactif par la glande thyroïde après 2 heures ne dépasse pas 20 %, après 24 heures - 50 %, l'accumulation de 99m Tc-pertechnétate après 2 heures ne dépasse pas 3 %. La différence d'accumulation d'iode radioactif et de technétium, qui n'entre pas dans la composition des hormones thyroïdiennes en 2 heures, permet de déterminer la quantité d'iode incluse uniquement dans la fraction organique, c'est-à-dire d'étudier la phase organique de métabolisme intrathyroïdien de l'iode.
L'étude de la phase transport-organique du métabolisme de l'iode (voir) est réalisée principalement en déterminant la concentration d'hormones thyroïdiennes et de globuline liant la thyroxine dans le plasma sanguin in vitro à l'aide de la méthode radioimmunologique. Cette méthode de diagnostic permet d'analyser biologiquement avec un haut degré de précision composants importants impliqué dans le processus pathologique. Dans ce cas, l'exposition du patient aux radiations est complètement éliminée.

Les méthodes d'évaluation de la structure de la glande thyroïde comprennent la tomodensitométrie (voir Tomodensitométrie), l'échographie (voir Diagnostic par ultrasons), l'analyse des radionucléides (voir) et la scintigraphie (voir), la biopsie par ponction (voir), ainsi qu'un certain nombre d'examens radiologiques spéciaux. méthodes - thyroïdographie aux rayons X (voir radiographie), thyroïdographie aux rayons X (voir électroradiographie), thyroïdolymphographie (Fig. 3), pneumothyroïdographie, angiothyroïdographie (voir angiographie). L'introduction de la tomodensitométrie, de l'échographie, de la numérisation des radionucléides et de la scintigraphie a conduit au fait que les méthodes spéciales de radiographie perdent de leur importance.
La tomodensitométrie fournit des images de la glande thyroïde et des tissus environnants. La glande thyroïde normale sur les tomographies transversales ressemble à deux ovales de structure homogène aux contours relativement lisses et bien délimités des tissus environnants. Avec les formations nodulaires dans la glande thyroïde, sa structure semble hétérogène. Les contours des formations dans le goitre nodulaire et le cancer de la thyroïde sont généralement moins nets que dans les tumeurs bénignes (adénome, kyste, etc.). Pour une tumeur maligne palpable, la tomodensitométrie permet de déterminer la forme, la taille, les contours, la structure du ganglion, la présence et l'étendue des métastases, ainsi que le degré d'implication des vaisseaux du cou et des tissus voisins dans l'évolution pathologique. processus. Il est conseillé de combiner l'utilisation de la tomodensitométrie pour le diagnostic des néoplasmes nodulaires et des processus pathologiques diffus de la glande thyroïde avec des tests radioimmunologiques, des ultrasons et des radionucléides.

La thyréographie des radionucléides (scanner et scintigraphie) occupe une place importante dans examen complet patients présentant une pathologie thyroïdienne. Grâce à cette méthode, la topographie de la glande thyroïde, sa taille et la nature de l'accumulation de radionucléides dans diverses parties de la glande sont évaluées. Le patient reçoit par voie orale 0,025-0,05 µCurie (1 - 2 MBq) de 131I ou 1,5-2,5 µCurie (60-100 MBq) de 99m Tc-pertechnétate et l'étude est réalisée après 2 et 24 heures. Normalement, le scanogramme montre clairement les contours de la glande thyroïde, de son lobe et de son isthme. Le maximum de radioactivité se produit au centre des lobes ; vers la périphérie des lobes, l'intensité du rayonnement diminue progressivement puis s'arrête brusquement. Les tailles des lobes et leur forme sont très variables. Le lobe pyramidal n'est le plus souvent pas détecté. Grâce à cette méthode, diverses anomalies dans la position de l'organe sont facilement identifiées. Dans les formes diffuses de goitre thyréotoxique (voir Goitre toxique diffus), le scanogramme montre une image agrandie de la glande thyroïde avec une répartition intense et uniforme du radionucléide. Dans d'autres cas (thyroïdite chronique, goitre mixte), une répartition inégale du radionucléide est observée. L'analyse et la scintigraphie permettent d'évaluer l'état fonctionnel des ganglions présents dans le tissu thyroïdien, ce qui est important pour le choix de la tactique thérapeutique. Ainsi, le substrat morphologique d'un ganglion « chaud » est le plus souvent un adénome toxique ou une hyperplasie non autonome du tissu thyroïdien (Fig. 4, a). Un nœud « froid » est une zone de tissu non fonctionnel, un kyste, un adénome, une métastase tumorale (Fig. 4, b). (Fig.4, a). Un nœud « froid » est une zone de tissu non fonctionnel, un kyste, un adénome, une métastase tumorale (Fig. 4, b).
Grâce à l'échographie unidimensionnelle et bidimensionnelle (échographie), vous pouvez obtenir des informations sur la taille de la glande thyroïde et ses zones individuelles. Normalement, l'échogramme révèle clairement les limites de la peau, du tissu sous-cutané, des fascias, des lobes de la glande thyroïde, des vaisseaux sanguins, des muscles, de la trachée et de la colonne vertébrale. Avec le goitre diffus, l'image de la glande thyroïde n'est pas modifiée, mais sa taille est augmentée. Dans la thyroïdite chronique et le goitre mixte, il existe une modification de la taille de la glande thyroïde et une hétérogénéité acoustique focale-diffuse de l'image de la glande avec une image normale des tissus environnants, si la trachée n'est pas déplacée. Le goitre nodulaire se caractérise par une image spécifique, en fonction de la structure du nœud. En règle générale, les ganglions denses, les adénomes, les zones de calcification et les kystes sont clairement définis sur fond de tissu thyroïdien inchangé. En cas de cancer de la thyroïde, le tableau échographique dépend de la nature et de l'étendue du processus pathologique. Si la tumeur ou ses métastases sont localisées, elles ne peuvent pas différer des ganglions denses ou de l'adénome. Lorsque les tissus adjacents sont impliqués dans le processus, des poches de compactage et des cordons y sont identifiés. L'échographie associée à la numérisation des radionucléides permet dans la plupart des cas de déterminer la taille et la structure de la glande thyroïde et de ses tumeurs, ce qui est important lors du choix de la méthode et de l'étendue de l'intervention chirurgicale.
La ponction de la glande thyroïde avec une aiguille fine (biopsie par ponction), réalisée à des fins diagnostiques, peut être réalisée en milieu ambulatoire. La fiabilité du diagnostic morphologique dépend de la précision de l'aiguille pénétrant dans la zone étudiée, c'est pourquoi on utilise la biopsie dite marginale, qui est réalisée soit sous le contrôle de l'échographie, soit selon les données de numérisation des radionucléides.
Dans le diagnostic des maladies thyroïdiennes, les tests fonctionnels (tests) effectués par l'administration de triiodothyronine, de thyréostimuline et de thyréolibérine (rifathiroine) sont d'une grande importance. Le test de suppression de la fonction thyroïdienne (test d'inhibition) est utilisé dans le diagnostic des formes effacées de thyréotoxicose (voir), du goitre endémique (voir Goitre endémique) et dans le diagnostic différentiel des ophtalmopathies. Pour ce faire, une étude des conditions d’accumulation est d’abord réalisée. La fiabilité du diagnostic morphologique dépend de la précision de l'aiguille pénétrant dans la zone étudiée, c'est pourquoi on utilise la biopsie dite marginale, qui est réalisée soit sous le contrôle de l'échographie, soit selon les données de numérisation des radionucléides.
Le test de stimulation de la fonction thyroïdienne est utilisé pour diagnostiquer l’hypothyroïdie primaire et secondaire ainsi que la fonction des ganglions présents dans la glande. La teneur en thyroxine dans le sérum sanguin est déterminée, après quoi la thyréostimuline est injectée par voie intramusculaire, puis un radionucléide (iode radioactif), suivi du dosage de la thyroxine et de l'étude de l'accumulation d'iode radioactif par la glande thyroïde. Chez les individus sains, l'accumulation d'iode radioactif par la glande thyroïde ou la teneur en thyroxine dans le sang dépasse de plus de 20 % les données initiales. À hypothyroïdie primaire Il n’y a aucune réponse à l’hormone stimulant la thyroïde. S'il existe des contre-indications au test des radionucléides, une méthode de détermination de la thyroxine dans le sérum sanguin est utilisée avant l'administration de l'hormone stimulant la thyroïde et 24 heures après son administration.
Le test de stimulation de l'hypophyse est utilisé pour diagnostic différentiel divers types d'hypothyroïdie. Dans ce cas, le taux initial de thyréostimuline dans le sérum sanguin est déterminé, puis la thyrolibérine est administrée (par voie intraveineuse ou per os), après quoi le taux de thyréostimuline dans le sérum sanguin est redéterminé. U personnes en bonne santé et avec l'hypothyroïdie primaire, le niveau d'hormone stimulant la thyroïde augmente considérablement par rapport au niveau initial. En cas d'hypothyroïdie secondaire (hypophysaire) et de goitre toxique diffus, il n'y a pas de réaction à la thyrolibérine. Si le patient présente toujours une réaction à la thyréostimuline exogène et à la thyréolibérine, il faut penser à une hypothyroïdie tertiaire (hypothalamique).
Pathologie
Selon la classification adoptée en 1961 lors du Congrès international des pays socialistes sur le problème du goitre endémique, anomalies congénitales de la glande thyroïde, goitre endémique (et crétinisme endémique), goitre sporadique, goitre toxique diffus, hypothyroïdie, maladies inflammatoires de la thyroïde glande (non spécifique et spécifique), on distingue les lésions et les tumeurs.
Défauts de développement
L'aplasie de la glande thyroïde est extrêmement rare et est due à une violation de la différenciation du rudiment embryonnaire en tissu thyroïdien. L'aplasie de la glande thyroïde est détectée dès la petite enfance. L'hypoplasie de la glande thyroïde est causée par un manque d'iode dans le corps de la mère. Cliniquement, un crétinisme est observé (voir). Le principal type de traitement est le traitement substitutif, qui est prescrit immédiatement après le diagnostic et même en cas de suspicion d'hypothyroïdie (voir). Un traitement rapide peut assurer le développement physique normal de l'enfant.
La préservation du canal thyréoglosse conduit souvent à la formation de kystes médians et de fistules du cou, de goitre de la racine de la langue. Les fistules et les kystes du canal thyréoglosse sont généralement reconnus au cours des dix premières années de la vie d’un enfant. Le traitement consiste en une excision complète des kystes. Le pronostic est favorable.
Le déplacement du rudiment médial de la glande thyroïde dans le médiastin provoque le développement d'un goitre intrasternal (voir Médiastin). Une anomalie du rudiment médial de la glande thyroïde provoque une dystopie du tissu thyroïdien dans la paroi de la trachée, du pharynx, du myocarde, du péricarde, du tissu adipeux du médiastin et des muscles squelettiques du cou. Les foyers dystopiques du tissu thyroïdien peuvent être une source de développement de tumeurs thyroïdiennes. La détection de tissu thyroïdien dans les ganglions lymphatiques du cou est considérée comme une métastase d'un cancer différencié de la thyroïde (voir la section Tumeurs ci-dessous). S'il y a un goitre ou une tumeur dans le tissu thyroïdien dystopique, un traitement chirurgical est indiqué.
Dommage
Les blessures fermées de la glande thyroïde sont rares (par exemple, compression du cou avec un nœud coulant lors d'une tentative de suicide) et se manifestent par la formation d'un hématome. Le repos et l'application locale de froid sont indiqués. Lorsque l'hématome se développe et qu'il y a des difficultés respiratoires, ils ont recours à l'arrêt du saignement et, si nécessaire, à une trachéotomie (voir).
Les blessures ouvertes de la glande thyroïde sont généralement associées à des blessures à d'autres organes du cou (voir) et s'accompagnent de saignements abondants (voir). Dans de tels cas, un traitement chirurgical urgent de la plaie (voir) avec résection économique de la partie endommagée de la glande, arrêt du saignement, suture des plaies avec drainage est nécessaire. Le pronostic dépend de l'étendue des dégâts.
Maladies
Des maladies peuvent survenir avec des signes d'augmentation de la fonction thyroïdienne (thyréotoxicose) ou de diminution de la fonction (hypothyroïdie). Dans certaines maladies de la glande thyroïde, les perturbations de sa fonction ne sont pas cliniquement détectées (voir Euthyroïdie).
La maladie thyroïdienne la plus courante est le goitre endémique (voir Goitre endémique), qui survient dans les zones géographiques où l'iode est insuffisant dans l'environnement. La maladie s'accompagne d'une hypertrophie diffuse, nodulaire ou mixte de la glande, dans la plupart des cas sans perturbation de sa fonction. La cause de la maladie est une carence en iode dans le corps. À usage prophylactique iodé sel de table et les préparations iodées, le taux de morbidité de la population est fortement réduit.
Le goitre sans dysfonctionnement prononcé de la glande thyroïde chez les personnes vivant dans des zones non endémiques est appelé goitre sporadique (voir Goitre sporadique).
Hypertrophie diffuse de la glande thyroïde avec son hyperfonctionnement, provoquant des troubles métaboliques et du développement changements pathologiques dans divers organes et systèmes, appelé « goitre toxique ». Il existe des goitres toxiques diffus, nodulaires et mixtes (voir Goitre toxique diffus).
Diminution de la fonction thyroïdienne - l'hypothyroïdie (voir) résulte de lésions de la glande thyroïde elle-même (hypothyroïdie primaire), de lésions de l'hypophyse (hypothyroïdie secondaire ou hypophysaire) ou de l'hypothalamus (hypothyroïdie tertiaire ou hypothalamique).
Les maladies inflammatoires de la glande thyroïde comprennent la thyroïdite non spécifique et spécifique (tuberculeuse, syphilitique, actinomycose) (voir). Il existe des aigus, des subaigus et thyroïdite chronique. La thyroïdite spécifique est extrêmement rare et constitue généralement une manifestation locale de maladies systémiques.
Tumeurs
Les tumeurs surviennent souvent dans le contexte d'une fonction accrue de stimulation de la thyroïde de l'hypophyse, ce qui provoque une prolifération de l'épithélium thyroïdien. La stimulation de la fonction de stimulation de la thyroïde de l'hypophyse peut être provoquée par une carence nutritionnelle en iode, des médicaments antithyroïdiens, une exposition à rayonnement ionisant(irradiation externe et interne), troubles dyshormonaux. Il existe des tumeurs bénignes et malignes de la glande thyroïde.
Tumeurs bénignes. Parmi les tumeurs bénignes, les adénomes sont plus fréquents (voir Adénome), généralement uniques, moins souvent multiples (goitre multinodulaire), constituant, selon Sloan et Franz (L. Sloan, W. Franz), 16 % de toutes les formations nodulaires du glande thyroïde. Fibrome (voir), tératome (voir), paragangliome (voir), hémangiome (voir), lipome (voir), myome (voir) sont rarement observés.
Sur la base de leur structure histologique, ils distinguent les adénomes trabéculaires (embryonnaires), tubulaires (fœtaux), microfolliculaires et macrofolliculaires (colloïdes). De multiples adénomes thyroïdiens peuvent avoir structure différente et différentes activités fonctionnelles.
Les adénomes ne dépassant pas 1 cm de diamètre n'apparaissent pas cliniquement. La tumeur est plus grande taille déterminé sous la forme d'un nœud rond et indolore à surface lisse, mobile lors de la déglutition. Au fur et à mesure de sa croissance et lorsqu'il est localisé derrière le sternum, l'adénome peut comprimer l'œsophage, la trachée, provoquant un essoufflement (voir), moins souvent - une dysphagie (voir).
Chez les patients atteints d'adénomes thyroïdiens, la fonction glandulaire n'est souvent pas altérée (voir Euthyroïdie). Avec l'adénome toxique, les phénomènes de thyréotoxicose se développent (voir).
Les adénomes trabéculaires et tubulaires n'absorbent pas l'iode radioactif. Les adénomes à structure folliculaire sont capables de capter l'iode à des degrés divers et de synthétiser des hormones thyroïdiennes.
La capacité d'un adénome à absorber l'iode est déterminée par un scanner de la glande thyroïde. Les adénomes qui ne captent pas ou faiblement l'iode radioactif apparaissent comme des ganglions « froids », et les adénomes qui captent activement l'iode radioactif apparaissent comme des ganglions « chauds » ou « chauds ».
Les cellules B peuvent être trouvées dans les adénomes. Une tumeur constituée entièrement de ces cellules est parfois considérée comme un adénome oncocytaire à grandes cellules. De tels adénomes sont le plus souvent monomorphes et ont une structure solide et folliculaire-solide. La possibilité de leur croissance invasive ne peut être exclue.
Les tumeurs similaires aux adénomes folliculaires, mais contenant un nombre variable de structures papillaires (papillaires), sont classées par certains chercheurs comme malignes. La question de la possibilité d'une variante bénigne d'une tumeur médullaire (adénome des cellules parafolliculaires) n'est pas complètement résolue.
Le diagnostic est établi sur la base des données d'un examen complet des patients, comprenant un laboratoire clinique, un radionucléide, des méthodes radiologiques, etc. Le rôle principal dans le diagnostic est joué par la ponction de la tumeur thyroïdienne avec une aiguille fine (biopsie par ponction) , suivi de examen cytologique le matériel reçu. Dans certains cas, un examen histologique urgent de la tumeur pendant l'intervention chirurgicale est nécessaire (cytodiagnostic peropératoire).
Le traitement des tumeurs bénignes de la thyroïde est chirurgical. L'opération consiste en une résection ou une ablation complète du lobe affecté de la glande (hémithyroïdectomie). L'opération d'énucléation de tumeur, autrefois très répandue, n'est pas utilisée actuellement.
Le pronostic du traitement radical est favorable dans la plupart des cas.
Tumeurs malignes. Selon A.I. Paches et R.M. Propp (1984), le cancer représente plus de 90 % de toutes les tumeurs malignes de la glande thyroïde. Les tumeurs non épithéliales, telles que le sarcome (voir), le lymphome malin (voir), l'hémangioendothéliome (voir Angioendothéliome), le tératome malin (voir), sont rares dans la glande thyroïde. Par structure et cours clinique elles ne diffèrent pas des tumeurs similaires d'autres organes.
Le cancer de la thyroïde est plus fréquent chez les femmes âgées de 40 à 60 ans. Il se développe souvent dans le contexte d'un goitre nodulaire à long terme (voir Maladies précancéreuses), mais il est possible de développer un cancer (voir) dans une glande inchangée, rarement - dans le contexte d'un goitre toxique diffus. La question du lien entre le cancer de la thyroïde et le goitre endémique n’est pas complètement résolue. Il existe des preuves du rôle oncogène de l'irradiation aux rayons X de la région de la tête et du cou pendant l'enfance et l'adolescence.
Il existe des cancers de la thyroïde différenciés et indifférenciés. Le cancer médullaire occupe une position intermédiaire entre eux. De plus, des tumeurs malignes provenant de l'épithélium métaplasique (carcinome épidermoïde) apparaissent dans la glande thyroïde.
Le groupe des tumeurs différenciées de la thyroïde comprend les cancers papillaire et folliculaire. Le cancer papillaire (adénocarcinome papillaire) est la forme de cancer de la thyroïde la plus courante (environ 65 %). Macroscopiquement, la tumeur est représentée par un nœud rond ou de forme irrégulière partiellement encapsulé. La taille de la tumeur varie considérablement. Il peut être très petit (détecté uniquement par examen microscopique) ou occuper la totalité de la glande et se propager aux tissus et organes environnants. L'examen microscopique révèle des structures papillaires (papillaires) caractéristiques qui constituent la majeure partie de la tumeur et des cavités kystiques remplies de colloïde ou de sang. Outre les structures papillaires, des structures folliculaires et, dans certains cas, des champs de cellules solides peuvent être trouvées dans la tumeur. Un signe caractéristique du cancer papillaire de la thyroïde est le dépôt focal de sels de calcium sous forme de corps psammotiques (voir).
Le cancer papillaire se caractérise par la capacité d'infiltrer la croissance avec germination dans la capsule de la glande thyroïde, dans les vaisseaux lymphatiques et, moins souvent, dans les vaisseaux sanguins. L'un des signes les plus typiques du cancer papillaire est la métastase aux ganglions lymphatiques régionaux.
Le développement de la tumeur est lent. Le cancer papillaire est généralement fonctionnellement inactif et ne s'accompagne pas de troubles endocriniens.
Le cancer folliculaire (adénocarcinome folliculaire) est observé moins fréquemment que le cancer papillaire. Macroscopiquement, il s'agit d'un nœud assez bien délimité de différentes tailles. Un petit ganglion est souvent découvert par hasard lors d'un examen histologique de tissu thyroïdien prélevé pour une autre raison, ou se manifeste cliniquement par des métastases dans les ganglions lymphatiques du cou, dans les poumons et les os. Au microscope, le cancer folliculaire est représenté par des structures folliculaires et trabéculaires, ainsi que par des croissances solides de cellules tumorales. Les cellules cancéreuses folliculaires peuvent ressembler aux thyrocytes d’une glande thyroïde normale. Une tumeur constituée de follicules hautement différenciés contenant du colloïde est moins maligne qu'une tumeur dans laquelle prédominent de petits follicules non colloïdaux, des structures trabéculaires et surtout solides.
Le cancer folliculaire est difficile à différencier morphologiquement de l'adénome folliculaire. L'invasion de cellules tumorales dans les vaisseaux et la capsule de la glande thyroïde ou la présence d'embolies de cellules tumorales dans les vaisseaux sanguins et lymphatiques permettent le diagnostic de cancer de la thyroïde.

Le cancer folliculaire se développe lentement, la tumeur est souvent fonctionnellement active. Un trait caractéristique est la métastase hématogène, qui touche principalement les poumons (Fig. 5) et les os.
Un type de cancer papillaire et parfois folliculaire de la thyroïde est ce qu'on appelle le cancer latent, ou microcarcinome sclérosant.
La tumeur est de très petite taille et présente généralement une structure papillaire présentant des symptômes prononcés de sclérose. Les métastases des ganglions lymphatiques régionaux du cou, qui étaient auparavant considérées à tort comme des tumeurs des glandes thyroïdiennes latérales aberrantes, sont souvent la seule manifestation clinique de ce type de cancer de la thyroïde.
Le cancer indifférencié de la thyroïde est l’une des tumeurs humaines les plus malignes ; il représente 5 à 20 % de tous les cancers de la thyroïde. Macroscopiquement, la tumeur est le plus souvent constituée de plusieurs ganglions, fusionnant souvent, sans limites claires. La tumeur est dense, de couleur blanchâtre lorsqu'elle est coupée, implique généralement toute la glande thyroïde et est fonctionnellement inactive. Le tableau microscopique du cancer indifférencié de la thyroïde est hétérogène. La tumeur peut être constituée de cellules petites et géantes, polymorphes ou fusiformes. Souvent, tous les types de cellules répertoriés se trouvent dans une seule tumeur, qui se développent dans des champs cellulaires continus et ne forment pas de structures folliculaires ou papillaires.
Caractérisé par le développement rapide de la tumeur primitive et des métastases généralisées. La tumeur envahit les tissus mous du cou, de la trachée, de l'œsophage, du nerf laryngé récurrent et du faisceau neurovasculaire du cou. Les complications graves sont les fistules œsophagiennes-trachéales (voir Bronches, tableau), l'asphyxie (voir) et les saignements (voir) des vaisseaux de la tumeur en désintégration.
Le cancer médullaire (cancer des cellules parafolliculaires) représente 2 à 4 % de tous les cancers de la thyroïde. Dans certains cas, la tumeur est génétiquement déterminée et est associée à un phéochromocytome (voir Chromaffinome) et à d'autres maladies du système endocrinien. Le développement du cancer médullaire est souvent précédé par hyperplasie focale cellules parafolliculaires. Macroscopiquement, le cancer médullaire est représenté par un ganglion tumoral dense sans limites claires, qui peut être soit de taille microscopique (microcarcinome), soit occuper toute la glande thyroïde et s'étendre au-delà de ses limites. La tumeur est rarement encapsulée, envahit souvent le tissu thyroïdien, infiltrant sa capsule et ses parois vaisseaux sanguins. Le tableau histologique du cancer médullaire de la thyroïde est hétérogène. Les cellules sont pour la plupart petites, rondes ou allongées ; des cellules fusiformes peuvent être présentes. Dans la plupart des cas, l’amyloïde est détectée dans les tissus du cancer médullaire. La microscopie électronique révèle des granules sécrétoires et des structures fibrillaires caractéristiques dans les cellules tumorales du cancer médullaire, comme dans les cellules parafolliculaires normales.
La tumeur est hormonalement active et produit de la calcitonine (voir). L'un des signes caractéristiques du cancer médullaire de la thyroïde est la diarrhée, provoquée par l'influence de facteurs humoraux sécrétés par la tumeur (calcitonine, sérotonine, etc.). Le cancer médullaire se caractérise par une évolution relativement longue, des métastases fréquentes aux ganglions lymphatiques régionaux et des récidives.
Le cancer épidermoïde de la thyroïde représente 1 à 3 % de toutes les tumeurs malignes de la thyroïde. Le plus souvent, des lésions secondaires de la glande thyroïde sont observées en raison de la propagation du carcinome épidermoïde à partir d'organes voisins (larynx, œsophage, etc.), ainsi qu'à des métastases provenant d'autres organes. Des zones de métaplasie squameuse peuvent survenir dans les cancers papillaires et folliculaires. La tumeur peut occuper toute la glande thyroïde et se propager aux tissus environnants. Au microscope, la tumeur a structure typique carcinome squameux. Wedge, l'évolution est extrêmement sévère, les métastases sont précoces et étendues.
La prévalence du cancer de la thyroïde est généralement évaluée par stade.
Stade I : petite tumeur encapsulée dans l'un des lobes de la glande. Stade II : a) la tumeur occupe la moitié de la glande, se développe dans sa capsule et est mobile ; b) une tumeur de taille identique ou inférieure avec des métastases régionales mobiles sur le cou d'un côté. Stade III : a) la tumeur occupe plus de la moitié ou la totalité de la glande, est fusionnée avec les organes voisins et a une mobilité limitée ; b) une tumeur de taille identique ou inférieure, mais avec des métastases bilatérales aux ganglions lymphatiques cervicaux. Stade IV : a) la tumeur se développe dans les tissus et organes environnants et reste immobile ; b) une tumeur de toute taille, mais avec des métastases à distance.
Le diagnostic du cancer de la thyroïde aux premiers stades est difficile, car une tumeur cancéreuse encapsulée ne présente pas de signes permettant de la distinguer d'un adénome. Ils utilisent un ensemble de méthodes, parmi lesquelles le rôle principal appartient à la biopsie par ponction (voir), les méthodes radiologiques (pneumothyroïdographie, artériographie, thyrolymphographie, tomodensitométrie), les méthodes radionucléides (voir Scanner, Scintigraphie), l'échographie (voir. Diagnostic échographique), thermographie (voir). Les données de laboratoire sont importantes pour le cancer médullaire, car elles nous permettent de déterminer augmentation de la sécrétion calcitonine. Dans les cas douteux, une intervention chirurgicale est indiquée, dont l'ampleur dépend des résultats d'un examen histologique urgent.
Le principal traitement du cancer de la thyroïde est la chirurgie. Les interventions chirurgicales pour le cancer de la thyroïde sont réalisées sous anesthésie endotrachéale (voir Anesthésie par inhalation). Le tissu affecté est retiré de manière extra-capsulaire avec ligature des vaisseaux partout, isolant les nerfs laryngés récurrents et les glandes parathyroïdes. Au stade I, l'hémithyroïdectomie est réalisée avec ablation de l'isthme ; au stade II - résection sous-totale de la glande ; aux stades III et IV - thyroïdectomie (voir). En présence de métastases mobiles dans les ganglions lymphatiques régionaux, accompagnée d'une thyroïdectomie, une excision de la gaine fasciale du tissu cervical est réalisée d'un ou des deux côtés. Pour les métastases peu déplacées dans les ganglions lymphatiques du cou d'un côté, l'opération Krile est indiquée (voir Opération Krile).
En complément de la méthode chirurgicale pour traitement combiné cancer indifférencié en période préopératoire ou postopératoire, la radiothérapie est utilisée (voir). À cancer différencié La radiothérapie est prescrite si elle est impossible à réaliser chirurgie radicale. La radiothérapie des tumeurs thyroïdiennes peut être utilisée comme type de traitement indépendant ou en association avec une hormonothérapie dans le traitement des tumeurs inopérables. tumeurs primaires, métastases aux ganglions lymphatiques régionaux et métastases à distance.
Dans les cas où la tumeur thyroïdienne et ses métastases n'accumulent pas ou faiblement 131 I, la radiothérapie est réalisée par irradiation externe. Le traitement est effectué à l'aide d'appareils de gamma-thérapeutique avec des sources de 60 Co, 137 Cs ou d'accélérateurs de haute énergie utilisant un rayonnement de bremsstrahlung ou électronique (voir Gamma thérapie), ainsi qu'en ingérant un médicament radiopharmaceutique marqué au 131I, qui s'accumule sélectivement dans l'atmosphère normale. tissu thyroïdien et dans les tumeurs de l'épithélium folliculaire qui conservent la fonction d'absorption de l'iode.
Pour l'irradiation préopératoire, des doses totales de 3 000 à 4 000 rad (30 à 40 Gy) sont recommandées, pour l'irradiation postopératoire - 4 000 à 5 000 rad (40 à 50 Gy). La zone d'irradiation comprend : la zone de la glande thyroïde, les zones des faisceaux neurovasculaires du cou et du médiastin antéro-supérieur. Pour le traitement des tumeurs inopérables et des métastases, une dose totale d'au moins 6 000 rad (60 Gy) est recommandée.
L'131I est principalement utilisé pour traiter les métastases à distance, les tumeurs primitives non résécables et les métastases régionales ayant une fonction absorbant l'iode. Le traitement à l'iode radioactif est effectué jusqu'à l'arrêt complet de l'accumulation d'iode dans les métastases.
L'hormonothérapie (voir) est indiquée après un traitement radical comme traitement de remplacement, ainsi que pour supprimer la production d'hormone thyréostimuline de l'hypophyse afin de prévenir les rechutes et les métastases. L'hormonothérapie est réalisée sous le contrôle des taux sanguins d'hormones thyroïdiennes et d'hormone thyréostimuline de l'hypophyse.
Le cancer de la thyroïde résiste aux médicaments anticancéreux modernes. Avec un processus largement répandu, un effet à court terme a été obtenu avec un traitement au diiodobenzotef et à l'adriamycine.
Le pronostic dépend du stade, de la structure histologique de la tumeur, du sexe et de l'âge des patients. Selon le Centre de recherche en oncologie de l'Union de l'Académie des sciences médicales de l'URSS, parmi les patients radicalement traités atteints d'un cancer de la thyroïde, le taux de survie à 5 ans était de 90 % et le taux de survie à 10 ans était de 86,4 %.
Opérations
L'intervention chirurgicale sur la glande thyroïde implique son ablation complète - thyroïdectomie (voir) ou partielle - résection de la glande thyroïde. À son tour, la résection de la glande thyroïde peut impliquer l'ablation d'un lobe de la glande (hémithyroïdectomie) ou une résection subtotale de la glande thyroïde, laissant 4 à 8 g de son tissu. Les indications d'une intervention chirurgicale sur la glande thyroïde sont les tumeurs de la glande thyroïde, la thyroïdite chronique à long terme (voir), le goitre toxique diffus (voir Goitre toxique diffus) et dans certains cas - le goitre nodulaire (voir Goitre sporadique, Goitre endémique). Il n’existe aucune contre-indication absolue à la chirurgie de la glande thyroïde.
Les interventions chirurgicales sur la glande thyroïde sont réalisées sous anesthésie locale ou endotrachéale. Le choix de la méthode d'anesthésie est individuel et dépend du volume, de la complexité technique de l'opération proposée, de l'âge et de l'état du patient.
Les patients atteints de goitre nodulaire et diffus qui sont dans un état euthyroïdien n'ont pas besoin de préparation particulière avant la chirurgie. En cas de goitre thyréotoxique, une préparation préopératoire est nécessaire afin de compenser les troubles provoqués par la thyréotoxicose et d'atteindre un état euthyroïdien, qui est la prévention d'une crise thyréotoxique en période postopératoire (voir Goitre toxique diffus).
Un ensemble d'outils utilisés pour préparation préopératoire, comprend les médicaments antithyroïdiens (voir), les corticostéroïdes (voir), ainsi que les médicaments qui normalisent l'activité cardiaque, les antihypertenseurs, les sédatifs (voir Antihypertenseurs, Sédatifs). Des antihistaminiques (pipolfen) et du promedol sont également prescrits en prémédication.
Les complications possibles qui surviennent immédiatement après la chirurgie peuvent être : parésie récurrente nerf laryngé, saignements, asphyxie ; peu de temps après l'intervention chirurgicale, une crise thyréotoxique (voir Crises), une hypoparathyroïdie, une hypothyroïdie peuvent survenir. En cas d'ablation complète de la glande thyroïde, un traitement substitutif est nécessaire pour prévenir l'hypothyroïdie, prescrit peu après l'opération.
La xénotransplantation de la glande thyroïde pour l'hypothyroïdie n'est pas utilisée en raison de sa faible efficacité ; l'autotransplantation est possible si la glande thyroïde retirée est préservée conditions spéciales(voir Transplantation).
Bibliographie: Aleshin B.V. À propos de certaines questions controversées de la cytophysiologie moderne de la glande thyroïde, Usp. moderne biol., tome 93, v. 1, p. 121, 1982 ; 0 n e, Le problème des cellules neuroendocrines et l'hypothèse du « système endocrinien diffus », ibid., vol. 98, siècle. 1, p. 116, 1984 : Aleshin B.V. et G u b s k et y V. I. Hypothalamus et glande thyroïde, M., 1983 ; Bomash N. Yu. Diagnostic morphologique des maladies thyroïdiennes, M., 1981 ; Boukhman A. II. Diagnostic radiologique en endocrinologie, M., 1 974 ; G o l b e r L. M. et K et n d-R ou V. I. Coeur thyrotoxique, M., 1972 ; G o lber JI. Métal. Pathogénèse troubles du mouvement pour la thyréotoxicose, M., 1980 ; G o r d i e n-co V. M. et Kozyritsky V. G. Ultrastructure des glandes du système endocrinien, Kiev, 1978 ; Zubovsky G. A. et Pavlov B. G. Numérisation des organes internes, M., 1973 ; Ivanitskaya V.I. et Shantyr V.I. Méthodes de rayonnement diagnostic et traitement du cancer de la thyroïde, Kiev, 1981 ; Klyach-ko V.R. Questions d'actualité traitement conservateur du goitre toxique, M., 1965; Kondalenko V. F., Kalinin A. P. et O d i n o k o v a V. A. Ultrastructure de la glande thyroïde humaine dans des conditions normales et en pathologie, Arkh. pathol., t. 32, n° 4, p. 25, 1970 ; L et n-denbraten L. D. et Naumov L. B. Méthodes d'examen aux rayons X des organes et systèmes humains, Tachkent, 1976 ; O r avec V. D. et M et r-khodzhaev A. X. Sélection de la méthode optimale pour le diagnostic mathématique des maladies thyroïdiennes, Probl. endocrinien., t. 24, n° 2, p. 23, 1978 ; Pache avec A. I. et Propp R. M. Cancer de la thyroïde, M., 1984 ; Raskin A. M. Processus auto-immuns dans la pathologie de la glande thyroïde, L., 1968 ; Guide d'endocrinologie clinique, éd. V.G. Baranova, p. 348, M., 1979 ; Slavno dans V.N. Études radio-isotopiques et radio-immunologiques de la fonction des glandes endocrines, Kiev, 1978 ; Strukov A.I. et Serov V.V. Anatomie pathologique, p. 26, M., 1979 ; Hormones thyroïdiennes, éd. Ya. X. Turakulova, p. 131, Tachkent, 1972 ; Physiologie du système endocrinien, éd. V.G. Baranova, p. 135, L., 1979 ; Thérapie endocrinienne tumeurs malignes, éd. BA Stolla, trad. de l'anglais, p. 401, M., 1976 ; Bernal J. a. Refetoff S. L'action de l'hormone thyroïdienne, Clin. Endocr., v. 6, p. 227, 1977 ; Chung S.T.a. o. Irradiation externe pour les tumeurs malignes de la thyroïde, Radiologie, v. 136, p. 753, 1980 ; Endocrinologie et métabolisme, éd. par Ph. Felig a. o., p. 281, N. Y. - Philadelphie, 1984 ; F u j i m o-t à propos de Y. Tumeurs thyroïdiennes, médecine asiatique. J., v. 25, p. 911, 1982 ; F u j i t a H. Structure fine de la glande thyroïde, Int. Tour. Cytol., v. 40, p. 197, 1975 ; Hormones dans le sang, éd. par S. H. Gray a. H.T. James, v. 1-3, L. a. o., 1979 ; Labhart A. Klinik der inneren Sekretion, B. u. à., 1971 ; M e n g W. Schilddriisenerkrankun-gen, Iéna, 1978 ; Rocmans P.A.a. o. La sécrétion hormonale par les cellules thyroïdiennes hyperactives n'est pas secondaire à la phagocytose apicale, Endocrinology, v. 103, p. 1834, 1978 ; Troisième colloque international sur la thyroïde, Cancer de la thyroïde, Acta endocr., suppl. 252, 1983 ; La thyroïde, éd. par S. C. Werner a* S. H. Ingbar, Hagerstown a. o., 1978 ; Cancer de la thyroïde, éd. par W. Duncan, B., 1980 ; La glande thyroïde, éd. par M. de Visscher, N.Y., 1980.
H.T. Starkova ; B. V. Aleshin (biochimique, physiol.), Yu. I. Borodine (an., hist., embr.), M. E. Bronstein, V. A. Odinokova (pat. an.), E. S Kiseleva (rad.), M. F. Logachev (péd. .), A. X. Mirkhodzhaev (met. recherche), R. M. Propp (onc.), A. A. Filatov (rad., loyer. ).